文|《未來跡》 林宇
又一批械字號產品明確監管類別!
日前,國家藥品監督管理局醫療器械標準管理中心對外發布《2023年第二次醫療器械分類界定結果匯總》(以下簡稱“《結果匯總》”)。其中匯總的醫療器械產品分類界定結果共249個,涵蓋了今年1月至4月醫療器械產品。
《結果匯總》中,有超20款醫美器械產品的判定界限有所變動,加上不久前發布的《2023年第一次醫療器械分類界定結果匯總》,此次監管部的動刀的目標很清晰——械字號的醫用敷料類產品。
醫用敷料變動最大
《FBeauty未來跡》梳理發現,一共有13類產品被納入II、III類醫療器械管理中,數量上以《第二次結果匯總》為主,占10款。整體來看,可以發現兩大關鍵點:
第一,7類產品可能被“剔”出械字號。
在最新《結果匯總》中,包含“重組人源化膠原蛋白”的重組膠原蛋白液體在內的7類產品建議不作為醫療器械管理。換而言之,此類產品可能會被“踢”出械字號范疇。
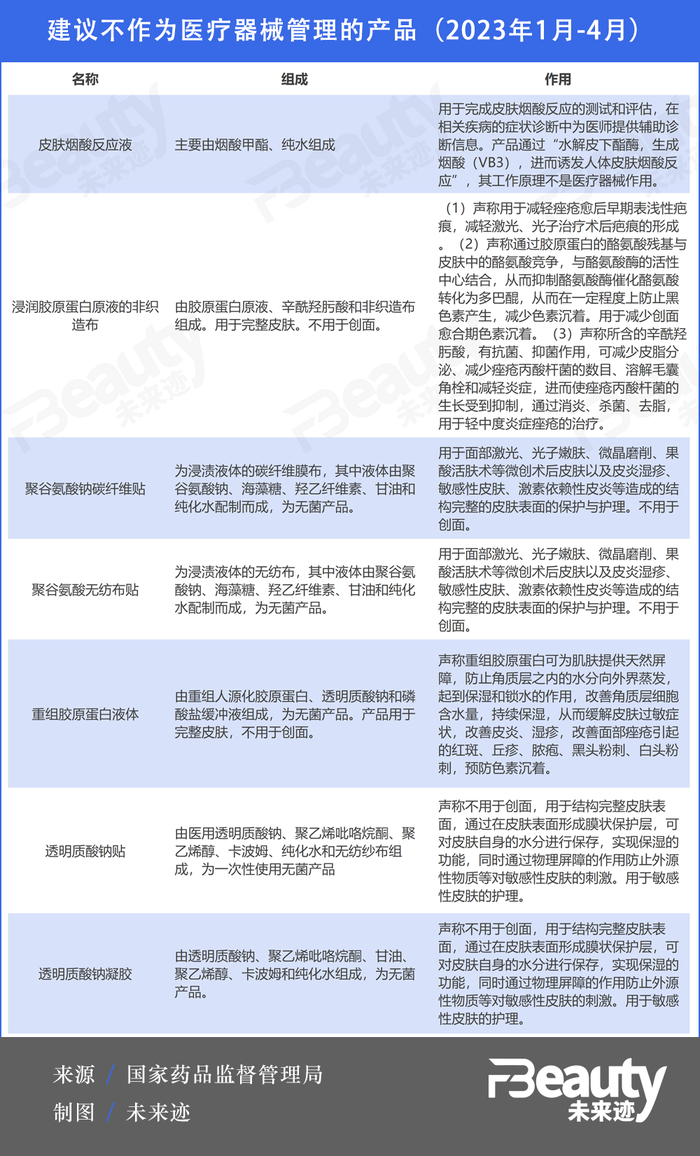
文件表述十分清晰,這7類產品因為不用于創面,或是只用于結構完整的皮膚表面的保護與護理而被建議不納入械字號管理。是否接觸創面、接觸創面的程度成為此次《結果匯總》對械字號分類調整的重要依據。
第二,部分醫用重組膠原蛋白類敷料列入II類醫療器械。
根據國家藥監局發布的《外科紗布敷料通用要求》定義,醫用敷料主要用于清潔覆蓋創面、吸收體內滲出液、為創面提供愈合環境,部分醫用敷料還可用于手術過程中支撐器官或組織,在醫療衛生領域起著重要作用。近些年來,醫用敷料在化妝品行業應用火熱。
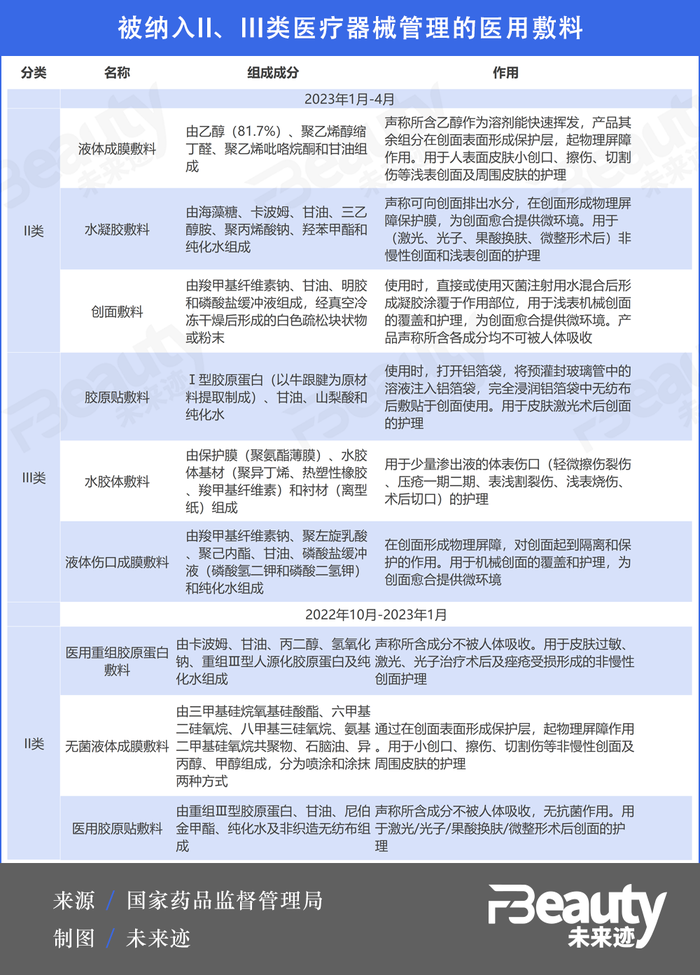
這兩次《結果匯總》中,一共新增9款醫用敷料,被列入II、III類醫療器械管理。其中膠原蛋白類敷料為監管重點。
其中,II類醫療器械中的三款醫用敷料都為《第一次結果匯總》發布,包含兩款膠原蛋白類敷料。一款名為“醫用重組膠原蛋白敷料”,由卡波姆、重組Ⅲ型人源化膠原蛋白、甘油等物質組成,用于皮膚過敏、激光、光子治療術后及痤瘡受損形成的非慢性創面護理;另一款名為“醫用膠原貼敷料”,由重組Ⅲ型膠原蛋白、甘油、尼伯金甲酯等物質組成,用于激光/光子/果酸換膚/微整形術后創面的護理。
除了膠原蛋白類原料之外,國家也正在對更多種類的醫用敷料展開嚴管,例如將用于激光、光子等醫美術后非慢性創面和淺表創面護理的水凝膠輔料納入III類醫療器械。
簡而言之,細微創面的醫用敷料被列為II類醫療器械管理,較大創面或較高風險的創面護理的醫用敷料被列入III類醫療器械嚴管。
細化分類,嚴格監管,已有企業提前布局調整
可以看出,國家正在逐步完善對醫用重組膠原蛋白的監管,并對管理范疇進行細化管理。而與此同時,械字號被擺到放大鏡下“微操式”管理,也意味著相關管理會更為嚴格。
首先“動刀”的地方是,將一些曾經被劃為III醫療器械的醫用敷料被降級為II類,包含“重組人源化膠原蛋白”的重組膠原蛋白液體以后可能不能作為醫療器械銷售。
事實上,械字號的分類對于此類產品有著重要的意義。
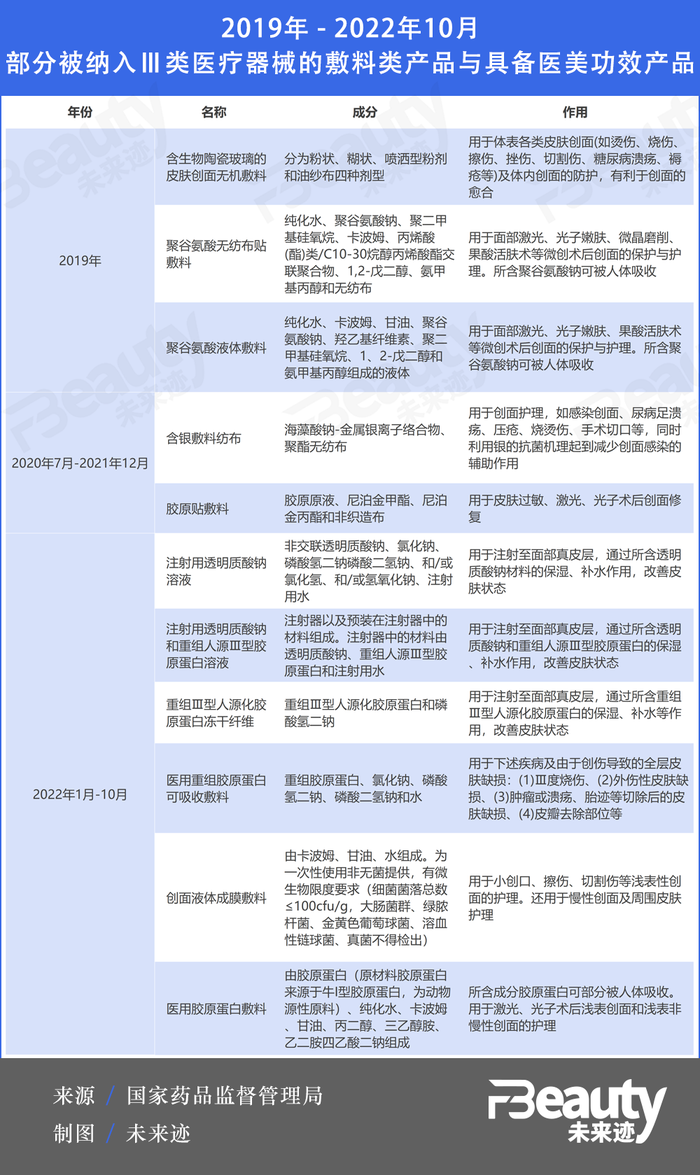
縱觀近些年的新增情況不難發現,自2020年開始,膠原蛋白類敷料就一直是III類醫療器械的“座上賓”。
此前,在2022年國家藥監局發布的1-6月《結果匯總》中,將“醫用重組膠原蛋白可吸收敷料”納入了III類醫療器械的管轄范圍中。但其應用范圍明確界定為:用于下述疾病及由于創傷導致的全層皮膚缺損:(1)Ⅲ度燒傷、(2)外傷性皮膚缺損、(3)腫瘤或潰瘍、胎跡等切除后的皮膚缺損、(4)皮瓣去除部位等。
與此同時,III類醫用敷料因壁壘較高和稀缺性,擁有更高的溢價空間,II類醫用敷料熱銷榜單中的產品價格帶在55元-200元之間,低于III類醫用敷料200元向上左右的價格,不乏部分品牌試圖用更高的械字號分類獲取更高的溢價。
《FBeauty未來跡》觀察發現,目前市面上的大多數醫用敷料類產品均屬于II類醫療器械,例如敷爾佳“白膜”“黑膜”、綻妍“藍膜”等,III類醫用敷料較少。
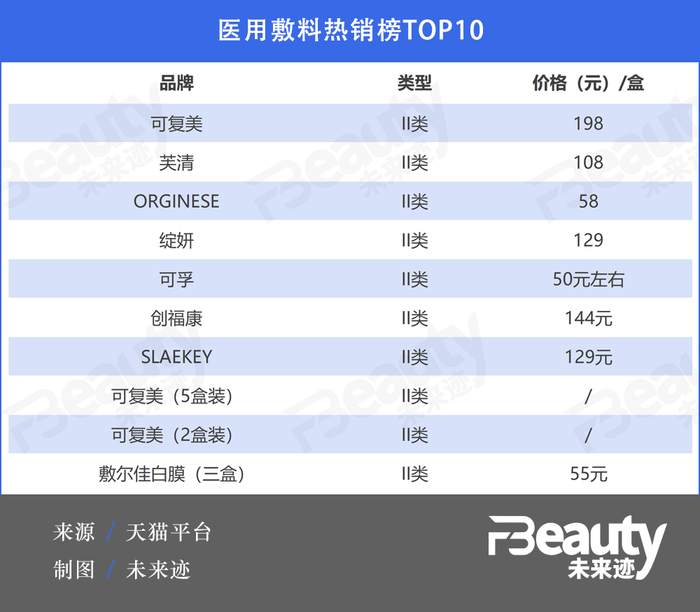
截至7月19日17點,從天貓醫用敷料熱銷榜來看,TOP10排名全都為II類醫用敷料,可復美、芙清位居前二,月銷量分別超20000、30000件。
但無論是當時還是現在,市面上大量存在的“重組膠原蛋白敷料”都主要用于激光、光子術后淺表創面和淺表非慢性創面護理,故而此類敷料的監管一直未有一個明確的“歸宿”。這兩次《結果匯總》,是在更加貼近市場的基礎上,明確了這類敷料的管轄范疇。
但械字號的分類與消費者的實際需求可能并不匹配,普通消費者的日常美容需求用II類產品即可滿足。荃智研究院創始人張太軍曾告訴《FBeauty未來跡》,僅用于日常面部護膚、無皮膚病或醫美術后需求的消費者,其實沒有必要用到III類醫用敷料產品。
法規調整越來越多了,更新越來越頻繁了,管理得越來越精準了,已經成為當前所有化妝品企業的共識。
2017年9月4日,國家藥監局正式發布新修訂的《醫療器械分類目錄》,此后每隔一段時間都會對醫療器械產品的分類界定結果進行匯總更新。2019年開始,敷料類產品陸續被納入III類醫療器械管控范疇。
2021年至2023年,國家藥監局相繼發布了《重組膠原蛋白類醫療產品分類界定原則的通告(2021年第27號)》、《重組人源化膠原蛋白原材料評價指導原則(征求意見稿)》、《重組人源化膠原蛋白》醫療器械行業標準。
2021年國家藥監局發布《關于醫療器械分類目錄動態調整工作程序的公告》之后,《醫療器械分類目錄》可由相關企業及機構提議,不定期進行動態調整。
同時,《分類目錄》根據需要進行調整,調整工作原則上每年不少于一次。此次《結果匯總》正是調整工作的進一步落實。
常態化更新且細節越來越多的《結果匯總》,已經在潛移默化中對市場產生影響。
《FBeauty未來跡》了解到,在法規公布前,已經注冊過的產品有五年的注冊有效期。廠家在這期間還可以繼續生產銷售,到期后才會受到管控。此外,上述人士還告訴《FBeauty未來跡》,廠家擁有一段時間的“過渡期”。例如注冊證書八月份到期的產品,八月份之前生產的東西仍可以正常售賣。
也有行業人士向《FBeauty未來跡》透露,近兩年市場上已經有一波生產械字號產品的企業正在轉向妝字號,他們似乎已經提前感知到,與其被越來越細分和精準的法規“趕回”妝字號,不如提前布局。
良性發展存在極大市場探索空間
對醫用敷料精細化、動態化管理,一方面源于市場亂象,另一方面則源于市場的快速發展。
中泰證券2021年發布的相關研報顯示,主要用于輕醫美術后的貼片式修護敷料市場規模近50億元,年均復合增長率(CAGR)達46%。預計2024年,醫用皮膚修復敷料消費量達9億片,醫美及敏感肌需求為主要成長拉力。
就在7月19日,國家藥品監督管理局發布《關于進一步加強和完善醫療器械分類管理工作的意見》中明確表示,“研究修訂《醫療器械分類規則》,為有序調整產品類別奠定基礎。針對新材料、高新技術等領域,聚焦監管熱點問題、共性問題和急需問題,在分類規則框架下研究細化分類界定指導原則,統一相關領域產品分類界定原則和尺度,服務產業高質量發展。”
在一個越來越熱,新技術、新材料迸發的市場里,需要有更及時、更具體的法規監管,職能部分對行業的重視程度也在不斷提升,也在打造一個更“接地氣”、更細致的法規體系。
但不變的是,“妝是妝、藥是藥”的監管思路在新規中得到了進一步的延伸。
目前來看,醫療器械和美容行業的交集,大面積集中在“敷料”市場。2020年過后,由于國家藥監局對“械字號”亂象的管控,持有II類和III類醫療器械證號的醫用敷料才能用于醫美或微整形后使用。(詳情可見:嚴上加嚴!醫用膠原蛋白敷料將被列入III類醫療器械監管)。
但職能機構依舊希望市場能夠在用于治療的“械”與日常護理的“妝”之間劃出清晰的界限,并在“械”中做出細分。部分企業試圖用“械”來塑造“專業、有效、安全”化妝品的形象錯位,有望通過械字號的級別調整和剔除得到“醫治”。
也有行業人士推測,法規的頻繁調整和監管的細致化、嚴格化,在不斷拉高械字號的門檻。
根據《醫療器械監督管理條例》,醫用敷料凡是聲稱無菌的,其管理類別最低為II類醫療器械;若接觸真皮深層或其以下組織受損的創面,或用于慢性創面,或可被人體全部或部分吸收的,其管理類別為第III類醫療器械。
II、III類產品的生產、監管以及流通環節,都對化妝品企業有極高要求。例如在生產環節,一位資深業內人士告訴《FBeauty未來跡》,一個II類產品申報注冊證的最短周期為八個月到一年,這個過程中需要付出大量人力物力財力成本。
此外,大部分II、III類產品需要進行臨床實驗;實際監管和流通中,II、III類的醫療器械監管執行單位層級更大,對經營場所和貯存條件要求更高,還需另外建立銷售記錄制度。一套流程下來,一般小型企業硬件和軟件都無法達到要求。
綠翊(廣州)技術服務有限公司技術法規研究負責人駱傳文告訴《FBeauty未來跡》,之所以對膠原類敷料把關嚴格,主要原因在于過去跟風亂象嚴重,導致質量普遍下滑。“通常來說,妝轉械的企業生產水平較低,均為10萬級車間+灌裝,并未有實際的原料研究,分子量研究,結構研究,生產過程活性控制研究,熱源等情況研究。”
械字產品敷料市場欣欣向榮,在一片向好的市場里,必然會有更多非理性和無序的“探索”,監管部門用法規“園藝剪”來修剪枝丫,修形狀、設門檻,顯得尤為重要。


