文|動脈網
昨晚的315晚會上,醫美亂象再次被曝光:妝字號產品被用于醫美注射,這一幕并非發生在無名小機構或美容院內,而是在大型展會上。
節目畫面顯示,在某大型展會現場,參加企業大多是生產美容醫療器械的廠家和化妝品公司。一些展商展出了用于填充、除皺、減肥、美白、補水等的注射針劑,這些原本應該按照三類器械管理的產品,卻只是妝字號。不少展臺內,甚至有工作人員當場為用戶進行注射。
化妝品公司工作人員在展會現場為消費者注射“妝字號”產品 圖片來源:315晚會截圖
央視記者在調查中發現,這類以化妝品名義銷售的美容針劑,價格不透明,利潤極其豐厚,讓從業者趨之若鶩。
一方面,展商工作人員表示產品銷售差價“起碼是乘以10”,這顯然是服務機構的獲利。另一方面,生產這類化妝品的公司也享受到市場“紅利”,一家參展公司的工作人員介紹,這些年市場上美容針劑的需求量大,銷售情況好,公司正在擴大生產規模,從老工廠的3層擴大到了新工廠的6層。
以往,社會對醫美行業不規范現象的關注主要集中在服務端,包括各類美容院、醫美診所甚至是大型整形美容醫院。而這次,曝光對象聚焦到了的上游,并且是亂象頻發的注射類醫美中上游,這也意味著,產業鏈在生產端有望迎來進一步凈化,促使醫美行業整體更加規范。
注射類醫美,正在快速滲透的巨大市場
事實上,注射類醫美已經形成了一個巨大市場。
注射類項目因效果明顯、操作簡便、恢復期短、價格相對低廉等特點,成為諸多用戶的入門選擇。
同時,注射類產品類型多樣、功效豐富,整體可分為填充類、萎縮類和其他類。其中,填充類包括膠原蛋白、玻尿酸、再生材料等針劑,可以使皮膚實現飽滿、立體的效果;萎縮類以肉毒素為主,可實現除皺、瘦臉、瘦身的功效。因此,產品可覆蓋廣泛的用戶群。
據頭豹研究院報告顯示,中國醫美行業消費以注射類醫美為主導,注射醫美消費占比達57%;但于韓國、美國等市場相比,中國注射醫美行業滲透率較低。2019年,中國注射醫美消費人次僅為14人/千人,遠低于其他主流國家,隨著醫美消費人群的增多,中國注射醫美行業存在較大發展潛力。
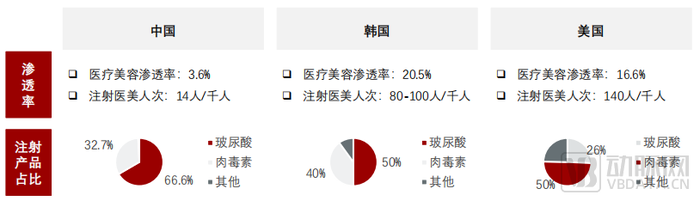
主要國家注射醫美市場比較,圖片來源:頭豹研究院
同時,存量市場中,因現有用戶對注射醫美產品的滲透率和復購頻率的提升,中國注射類醫美市場在復購需求影響下仍存在較大存量增長空間。
華熙生物、愛美客、昊海生科等公司在注射類醫美領域耕耘已久,布局了豐富的注射類醫美產品,相應產品也呈現出可觀的收入規模。
最新年報顯示,2022年,愛美客旗下溶液類與凝膠類注射產品收入雙雙增長。其中,溶液類注射產品收入12.93億元,同比增長 23.57%;凝膠類注射產品收入6.38億元,同比增長65.61%。
隨著注射類項目在用戶中的滲透擴大,產品銷售規模將進一步增長。據弗若斯特沙利文和東興證券測算,到2027年,我國注射類醫美市場規模有望達到1255億元。
產品體系從玻尿酸,到肉毒素、再生填充
玻尿酸是注射類醫美發展時間最長的“網紅”產品之一,被廣大消費者和準消費者熟知。
截至目前,昊海生科的玻尿酸產品已研發至第四代。其中,第一代玻尿酸產品“海薇”是國內首個獲得國家藥監局批準的單相交聯注射用透明質酸鈉凝膠,主要定位于大眾普及入門型玻尿酸。第二代玻尿酸產品“姣蘭”主要市場定位為中高端玻尿酸,主打“動態填充”功能,第三代玻尿酸產品“海魅”具有線性無顆粒特征,市場定位為高端玻尿酸,主打“精準雕飾”功能。2022年,第四代有機交聯玻尿酸產品的臨床試驗正在推進。
作為幾乎與玻尿酸齊名的產品,肉毒素也已吸引業內參與者紛紛布局。
康哲藥業與韓國BMI就A型肉毒素100U凍干粉針劑達成合作,訂立了許可、合作和經銷協議。昊海生科則投資了Eirion,布局“外用涂抹+經典注射”肉毒素產品線等。
初創公司方面,2023年1月,君合盟生物完成近億元A+輪融資,其研發管線布局在代謝、醫美等廣闊市場前沿蛋白藥物領域,其中,先導產品就包括重組A型肉毒素。
現階段國內市場已有衡力、保妥適、吉適、樂提葆等幾款肉毒素產品獲批,隨著更多參與者將入,行業將更加火熱。
與此同時,注射類醫美正在步入“再生時代”。
再生材料是能夠刺激人體纖維細胞和膠原蛋白再生的新型材料。國內目前主流的醫美再生材料包括聚左旋乳酸(PLLA)、聚己內酯(PCL)等,隨著生產技術的進步,再生材料應用場景從醫療端逐漸拓展至醫美端,并推動醫美注射產品豐富和功效優化。
在此之前,以PLLA為核心成分的童顏針、以PCL為核心成分的少女針,在國外醫美市場已上市和使用多年。根據國際美容整形外科學會(ISAPS)發布的調查報告,2016-2020年,注射類醫美項目中,PLLA皮膚填充劑在全球市場療程量增長最快。
2021年以來,國內三款基于再生材料的醫美產品獲批上市,包括華東醫藥的伊妍仕少女針、圣博瑪的艾維嵐童顏針、愛美客的濡白天使童顏針。
作為填充針劑,再生材料的效果比玻尿酸更自然和持久,驅動醫美注射從填充時代邁入“再生時代”,也迎合了求美者的迫切需求。
基于不同材料形成的產品體系,進一步豐富了注射類項目的功效,有助于這一市場的快速增長。
監管延伸至生產端,將加快市場凈化
龐大的市場規模、日漸豐富的產品品類、更加精細的產品功效,讓合規經營企業發展迅速,也讓不法廠家和商家嗅到“商機”。
按國家藥監局規定,注射類醫美產品按三類器械管理,包括大眾所熟知的水光針。也就是說,一款產品從啟動研發到上市,需經過較長周期、投入大量資金,需通過臨床試驗驗證安全性和有效性。“械字號”與“妝字號”的最大區別也正在于此。
例如,2022年,愛美客研發投入金額達1.73億元,同比增長 69.20%,占營業收入的8.93%。2022年上半年,華熙生物研發投入1.79億元,占營業收入的6.11%;昊海生科研發投入7671萬元,占營業收入的7.93%。
不斷將營業收入中一定比例的資金用于產品研發、豐富產品線,使得公司持續擁有契合市場的產品布局,才能在合規的前提下,使企業具有競爭力。從宏觀層面看,良性的市場競爭也應該如此。
很顯然,以“妝字號”之名,行“械字號”之實,擾亂了良性的市場競爭。
事實上,對于注射類醫美項目的違規整治,監管部門一直高度重視。
面向消費者,國家藥監局發布了《注射醫療美容醫療器械消費風險提示》:我國已批準上市的注射用交聯透明質酸鈉凝膠、膠原蛋白植入劑等整形用注射填充物類醫療器械,在使用過程中需要通過注射針等醫療器械注射到真皮層或皮下組織。按照有關規定,相關注射必須在有資質的美容醫療機構內,由具有從事相關臨床學科工作經歷的執業醫師操作,并嚴格按照醫療器械說明書進行使用。
面向服務機構,監管部門多次進行專項整治。2022年11月,工業和信息化部、市場監管總局、中央網信辦等18部門聯合印發了《進一步提高產品、工程和服務質量行動方案(2022—2025年)》,其中提出“按年度提出國家醫療質量安全改進目標,推動醫療服務質量持續改進。加強醫療美容綜合監管執法。”
2022年12月,國家藥監局通報了7起醫療美容藥品醫療器械違法案例,其中就包括:嘉興市柏惠醫療美容門診部有限公司從非法渠道購進藥品、使用未依法注冊醫療器械注射用透明質酸鈉凝膠。
此次315晚會曝光的對象主要是生產銷售端參與者,將促進主管部門進一步延伸監管范圍、加大監管力度。
據媒體報道,3月15日當晚,廣州市市場監督管理局就發布情況通報稱,央視315晚會曝光了醫療美容行業投訴的問題,其使用的產品涉及廣州生產企業,廣州市、區市場監管部門已立即行動,第一時間趕至現場,對涉事企業進行核查處置,對涉事產品進行封存、組織開展抽檢。后續依法依規嚴查嚴處情況,將及時向社會通報。
當違規產業鏈從服務端到生產端都得以清理,那些合規生產和經營的企業、服務機構才能獲得更好的市場發展空間,構成更加良性的市場生態。


