文|動(dòng)脈網(wǎng)
近年來(lái),在政策助力和資本扶持下,我國(guó)醫(yī)療器械行業(yè)整體水平不斷提升,從國(guó)內(nèi)醫(yī)療器械行業(yè)從從一窮二白到各領(lǐng)域全面開(kāi)花,并逐步突破核心領(lǐng)域及關(guān)鍵技術(shù),甚至在某些領(lǐng)域達(dá)到了國(guó)際先進(jìn)水平。
當(dāng)然,這并不代表我國(guó)醫(yī)療器械行業(yè)可以就此高枕無(wú)憂,走上坦途。由于起步較晚,我國(guó)在高端醫(yī)療器械的創(chuàng)新上距離全球先進(jìn)水平仍有相當(dāng)差距。看清差距,或許更有利于今后的對(duì)癥下藥。
近日,F(xiàn)DA和NMPA先后發(fā)布了2022年醫(yī)療器械創(chuàng)新方面的總結(jié)。動(dòng)脈網(wǎng)據(jù)此進(jìn)行了整理,希望能夠厘清我國(guó)與全球先進(jìn)水平在醫(yī)療器械創(chuàng)新方向上的不同,以為行業(yè)參考。
累積納入760款僅62款獲準(zhǔn)上市,F(xiàn)DA“突破性設(shè)備”寬進(jìn)嚴(yán)出
歷經(jīng)多年發(fā)展,美國(guó)在醫(yī)療器械創(chuàng)新上的地位無(wú)可撼動(dòng)。一方面,美國(guó)擁有全球絕大多數(shù)頂尖醫(yī)療器械公司,在研發(fā)上有海量投入;另一方面,通過(guò)一系列頂層建設(shè),美國(guó)掃清了高校創(chuàng)新的障礙,使其能力得到極大釋放。

除此以外,監(jiān)管機(jī)構(gòu)也尤為重視鼓勵(lì)創(chuàng)新。作為醫(yī)療器械上市的審批單位,F(xiàn)DA從2018年開(kāi)始設(shè)立了“突破性設(shè)備”計(jì)劃,用以鼓勵(lì)創(chuàng)新醫(yī)療器械的發(fā)展。其范圍涵蓋了上市前批準(zhǔn)申請(qǐng)(PMA),上市前通知(510(k))或De Novo分類申請(qǐng)框架下進(jìn)行審核。
簡(jiǎn)單而言,PMA風(fēng)險(xiǎn)等級(jí)大體與國(guó)內(nèi)3類證相當(dāng),通常需要完成臨床試驗(yàn)與實(shí)驗(yàn)室測(cè)試。510(k)風(fēng)險(xiǎn)等級(jí)則與2類證相當(dāng),其基本過(guò)程是通過(guò)提交與市面已獲批醫(yī)療器械的對(duì)比,證明申請(qǐng)器械實(shí)質(zhì)性等同參照器械即可。
所謂實(shí)質(zhì)性等同指申請(qǐng)器械至少與已上市產(chǎn)品同樣安全或更安全,且不能引起有關(guān)安全及有效性的任何問(wèn)題。因此,這一流程可以大幅提升獲批效率。
若中低風(fēng)險(xiǎn)醫(yī)療器械沒(méi)有找到可參照的實(shí)質(zhì)性等同器械,則可以申請(qǐng)進(jìn)入De Novo通道。一旦進(jìn)入De Novo通道,則后續(xù)可以進(jìn)一步提交510(k)申請(qǐng),類似于我國(guó)的2類創(chuàng)新醫(yī)療器械。
“突破性設(shè)備”可以明顯縮短這些醫(yī)療器械的獲批上市時(shí)間,因此它取代了之前的快速訪問(wèn)途徑(EAP——Expedited Access Pathway)和優(yōu)先審查(PR——Priority Review)。
要想進(jìn)入“突破性設(shè)備”清單,則需要滿足下列標(biāo)準(zhǔn)。

基于美國(guó)醫(yī)療器械在全球的領(lǐng)先地位,F(xiàn)DA的“突破性設(shè)備”事實(shí)上代表了全球醫(yī)療器械創(chuàng)新的頂尖水平。
除了“突破性設(shè)備”,F(xiàn)DA還在2021年設(shè)立了“醫(yī)療器械安全技術(shù)計(jì)劃”(STeP——Safe Technology Program),用于覆蓋不符合突破性器械計(jì)劃的醫(yī)療器械。這些器械雖然有其創(chuàng)新之處,但所針對(duì)的疾病往往并不嚴(yán)重,達(dá)不到“突破性設(shè)備”的緊迫程度。
從2015年開(kāi)始截至2022年12月31日(之前通過(guò)EAP計(jì)劃納入的器械也被FDA計(jì)算在內(nèi)),共計(jì)有760款醫(yī)療器械被納入“突破性設(shè)備”名單。這其中,除了8款由主管生物制品的CBER(生物制品評(píng)價(jià)與研究中心)通過(guò),其余752款均由主管醫(yī)療器械和數(shù)字醫(yī)療的CDRH通過(guò)申請(qǐng)。
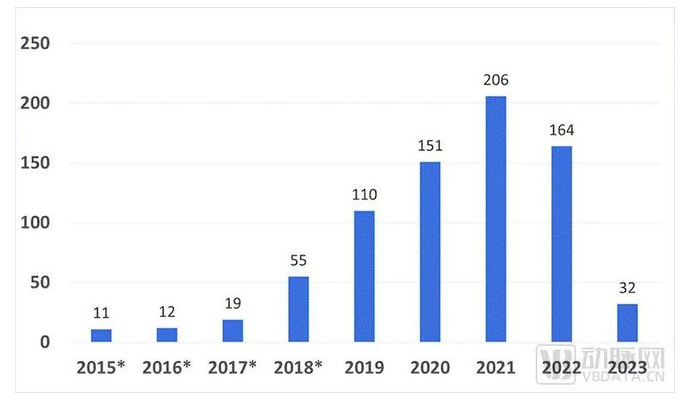
歷年FDA“突破性設(shè)備”分布(本圖為按FDA財(cái)年劃分,對(duì)應(yīng)截至自然年時(shí)間為2022年12月31日,圖片來(lái)自FDA官網(wǎng))
如果按領(lǐng)域劃分,“突破性設(shè)備”共可被分為20個(gè)領(lǐng)域。這其中,針對(duì)心血管的“突破性設(shè)備”數(shù)量最多,歷年共有171款。其次則是針對(duì)神經(jīng)領(lǐng)域的“突破性設(shè)備”,共有137款。在這之后則是骨科(87)、腸胃科(60)和整形外科(53)。
這5個(gè)領(lǐng)域的“突破性設(shè)備”累計(jì)數(shù)量達(dá)到了508款,占比高達(dá)66.8%。這也代表了目前全球頂尖醫(yī)療器械創(chuàng)新主要的方向和趨勢(shì)。
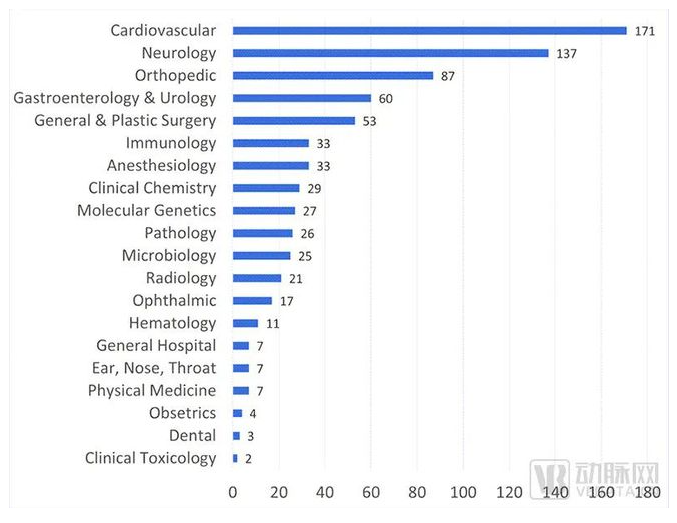
FDA“突破性設(shè)備”數(shù)量分布(按領(lǐng)域劃分,截至2022年12月31日,圖片來(lái)自FDA官網(wǎng))
不過(guò),雖然入選名單看似龐大,但真正能夠獲準(zhǔn)上市的其實(shí)并不多。從2015年至今,一共也僅有62款“突破性設(shè)備”獲得了FDA的上市批準(zhǔn),通過(guò)率其實(shí)僅有8.9%而已。
2022年,一共有19款“突破性設(shè)備”最終獲準(zhǔn)上市。這其中,也包括了首個(gè)用于阿爾茨海默癥早診的IVD設(shè)備、首次運(yùn)用眼動(dòng)追蹤技術(shù)評(píng)估兒童ASD的設(shè)備以及全球唯一可用于DCD心臟移植的系統(tǒng)。
● 首個(gè)用于阿爾茨海默癥早診的IVD設(shè)備
富士瑞必歐的Lumipulse G ?-amyloid ratio是首個(gè)用于早期檢測(cè)與阿爾茨海默癥相關(guān)淀粉樣斑塊的體外診斷測(cè)試設(shè)備,可用于評(píng)估55歲及以上認(rèn)知障礙患者認(rèn)知能力下降的原因是否與阿爾茨海默癥相關(guān)。
Lumipulse測(cè)試則通過(guò)測(cè)量人腦脊液(CSF)中發(fā)現(xiàn)的β-淀粉樣蛋白1-42和β-淀粉樣蛋白1-40(可以積聚并形成斑塊的特定蛋白質(zhì))濃度的比例,并與其他臨床評(píng)估結(jié)合使用幫助醫(yī)生初步篩查患者腦部是否可能存在淀粉樣斑塊,進(jìn)而再?zèng)Q定下一步診斷和治療。
在這一創(chuàng)新醫(yī)療器械獲準(zhǔn)上市之前,醫(yī)生只能使用影像設(shè)備來(lái)檢測(cè)認(rèn)知障礙患者大腦中的淀粉樣斑塊。對(duì)于患者來(lái)說(shuō),影像掃描耗費(fèi)時(shí)間且價(jià)格昂貴,也存在輻射風(fēng)險(xiǎn)。Lumipulse G ?-amyloid ratio僅需一天就可完成測(cè)試并出具報(bào)告,價(jià)格相對(duì)便宜,且沒(méi)有潛在的輻射風(fēng)險(xiǎn),可為阿爾茨海默癥的早期診斷提供很好的選擇。
● 首次運(yùn)用眼動(dòng)追蹤技術(shù)評(píng)估兒童ASD
Earlitec Diagnostics的Earlipoint System創(chuàng)新性地采用了眼動(dòng)追蹤技術(shù),可用于16-30個(gè)月兒童的ASD(孤獨(dú)癥譜系障礙)評(píng)估。
該系統(tǒng)利用社會(huì)-視覺(jué)參與動(dòng)態(tài)量化(DQSVE)可以捕捉兒童在觀看一系列描述兒童社交互動(dòng)短視頻場(chǎng)景時(shí)難以被人眼察覺(jué)的細(xì)微行為來(lái)對(duì)兒童注意力和響應(yīng)能力進(jìn)行評(píng)估。評(píng)估由訓(xùn)練有素的技術(shù)人員進(jìn)行,應(yīng)用場(chǎng)景為一名兒童觀看一系列描述兒童之間社交互動(dòng)的短視頻。
眼動(dòng)追蹤技術(shù)以每秒120次的速度評(píng)估各個(gè)焦點(diǎn),然后將每個(gè)數(shù)據(jù)點(diǎn)與臨床驗(yàn)證數(shù)據(jù)庫(kù)中的數(shù)千個(gè)離散測(cè)量值進(jìn)行比較,利用專利分析技術(shù)將結(jié)果與預(yù)期年齡參考指標(biāo)對(duì)比,并提供與社會(huì)殘疾水平以及語(yǔ)言和非語(yǔ)言能力相關(guān)的EarliPoint嚴(yán)重性指數(shù),進(jìn)而實(shí)現(xiàn)ASD患兒的早期識(shí)別。
● 全球唯一可用于DCD心臟移植的系統(tǒng)
TransMedics自主研發(fā)的便攜式器官保存系統(tǒng)Organ Care System (OCS) Heart System是首個(gè)能將自然死亡后捐贈(zèng)的心臟保存在溫暖的跳動(dòng)狀態(tài)下的裝置,也是FDA唯一批準(zhǔn)的用于保存標(biāo)準(zhǔn)和擴(kuò)大標(biāo)準(zhǔn)供體心臟的設(shè)備,還是全球唯一可用于DCD心臟移植的系統(tǒng)。
器官移植的時(shí)效性極為重要,如心臟僅能承受8小時(shí)的冷缺血時(shí)間。若器官長(zhǎng)期處于冷缺血狀態(tài),將會(huì)導(dǎo)致永久性損傷。臨床上通常采用“靜態(tài)冷藏法”來(lái)保存器官。即從人體摘取器官后先向器官內(nèi)注入保存液,而后將器官放入冷藏箱內(nèi),利用低溫來(lái)減緩器官的新陳代謝過(guò)程。
但這種方式已經(jīng)逐漸暴露出一些問(wèn)題,如器官長(zhǎng)時(shí)間冷藏后功能受損,且醫(yī)生無(wú)法監(jiān)測(cè)器官功能狀態(tài)等。因此,利用機(jī)械灌注在體外為器官?gòu)?fù)制一個(gè)體內(nèi)環(huán)境,從而保持器官的正常代謝是器官保存技術(shù)的新方向。
Organ Care System (OCS) Heart System通過(guò)向器官灌注溫暖、含氧、營(yíng)養(yǎng)豐富的血液,模擬人體新陳代謝的狀態(tài),以減少器官缺血時(shí)間,維持器官活性。醫(yī)生還可以通過(guò)該系統(tǒng)實(shí)時(shí)監(jiān)測(cè)器官的功能與活性,評(píng)估其是否可用于移植。
全年納入68款獲批55款,我國(guó)創(chuàng)新醫(yī)療器械審批創(chuàng)歷史新高
無(wú)獨(dú)有偶,NMPA也在近期發(fā)布了我國(guó)2022年醫(yī)療器械總結(jié),并對(duì)創(chuàng)新醫(yī)療器械注冊(cè)審批進(jìn)行了回顧。
2022年,共有343款醫(yī)療器械申請(qǐng)創(chuàng)新醫(yī)療器械特別審批,比2021年增加37.8%。其中68款獲準(zhǔn)進(jìn)入創(chuàng)新醫(yī)療器械特別審查程序,比上一年略多。通過(guò)創(chuàng)新醫(yī)療器械通道獲批55款,比上一年大幅增加57.1%。
從2014年至2022年,NMPA共批準(zhǔn)189個(gè)3類創(chuàng)新醫(yī)療器械。其中,境內(nèi)創(chuàng)新醫(yī)療器械涉及15個(gè)省的134家企業(yè),進(jìn)口創(chuàng)新醫(yī)療器械涉及2個(gè)國(guó)家的8個(gè)企業(yè)。
2019年是我國(guó)創(chuàng)新醫(yī)療器械新規(guī)開(kāi)始實(shí)施的第一年,從彼時(shí)起,我國(guó)醫(yī)療器械創(chuàng)新開(kāi)始逐步成長(zhǎng),無(wú)論是申請(qǐng)數(shù)量、進(jìn)入程序數(shù)量和最終獲批的數(shù)量都在逐年增加。2022年,各項(xiàng)指標(biāo)都創(chuàng)下了歷史新高,甚至超越了新規(guī)實(shí)施前巔峰的2017年(進(jìn)入程序)和2018年(申請(qǐng)數(shù)量)。從數(shù)量上來(lái)看,醫(yī)療器械行業(yè)的創(chuàng)新熱情的確得到了激發(fā)。
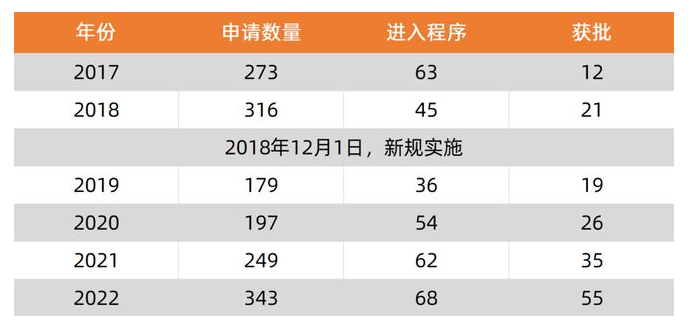
事實(shí)上,這僅是國(guó)家局對(duì)3類創(chuàng)新醫(yī)療器械的統(tǒng)計(jì)。如果加上由地方局審批的2類創(chuàng)新醫(yī)療器械,數(shù)量將會(huì)更加龐大。根據(jù)動(dòng)脈網(wǎng)的不完全統(tǒng)計(jì),2022年各地方局納入創(chuàng)新醫(yī)療程序的2類醫(yī)療器械至少為89款。
需要指出的是,各地對(duì)創(chuàng)新醫(yī)療器械的審批不完全相同。比如,有的地區(qū)特別設(shè)置了2類創(chuàng)新醫(yī)療器械審批程序,有的地區(qū)則是在優(yōu)先審批醫(yī)療器械中包含了創(chuàng)新醫(yī)療器械。
單純從數(shù)量上而言,我國(guó)醫(yī)療器械創(chuàng)新的確呈現(xiàn)出朝氣蓬勃的景象。不過(guò),由于我國(guó)醫(yī)療器械行業(yè)尚需進(jìn)一步發(fā)展,相當(dāng)數(shù)量的“國(guó)內(nèi)首創(chuàng)”創(chuàng)新醫(yī)療器械仍處于填補(bǔ)國(guó)內(nèi)空白的階段,能夠達(dá)到“各項(xiàng)性能指標(biāo)達(dá)到國(guó)際同品種器械水平”評(píng)價(jià)的器械也并不算多。總體而言,我國(guó)醫(yī)療器械距離全球先進(jìn)水平仍有一定差距也是客觀事實(shí)。
不過(guò),2022年,仍有幾款值得一提的獲批創(chuàng)新醫(yī)療器械,在技術(shù)水平和設(shè)計(jì)上達(dá)到了行業(yè)領(lǐng)先水平,并在NMPA給出的評(píng)價(jià)中予以體現(xiàn)。
● 全球獨(dú)一,首個(gè)通過(guò)體內(nèi)振動(dòng)改善功能性便秘的膠囊機(jī)器人
這一產(chǎn)品由上海安翰醫(yī)療技術(shù)有限公司推出,于2018年申請(qǐng)成功納入創(chuàng)新醫(yī)療器械審批流程,并于2022年2月最終獲批,被NMPA認(rèn)為是“同類首個(gè),目前國(guó)內(nèi)外尚無(wú)同類產(chǎn)品上市”。
目前,便秘治療雖然有多種方法可供選擇,但存在患病率高、治療副作用大、復(fù)發(fā)率高和病人滿意度低的情況。這種一次性使用的消化道振動(dòng)膠囊可通過(guò)振動(dòng)對(duì)結(jié)腸壁進(jìn)行刺激,促進(jìn)結(jié)腸蠕動(dòng),為藥物治療效果欠佳的成人功能性慢性傳輸型便秘提供非藥物治療的全新治療辦法。
● 全球首款雙源、雙探測(cè)器口腔CBCT
北京朗視儀器股份有限公司的這款創(chuàng)新醫(yī)療器械于2020年納入創(chuàng)新醫(yī)療器械審批程序,并于2022年7月獲批,“是全球首款雙源、雙探測(cè)器的口腔CBCT產(chǎn)品”(NMPA評(píng)價(jià))。其核心技術(shù)為雙源成像技術(shù),通過(guò)小焦點(diǎn)、高功率X射線管頭和高分辨率探測(cè)器提升空間分辨率,在滿足口腔頜面部成像需求的基礎(chǔ)上,為耳鼻喉科疾病提供X射線錐形束體層攝影檢查。
它具備大、小兩種視野成像系統(tǒng),大視野成像系統(tǒng)可用于口腔頜面部、鼻部和咽喉部氣道的常規(guī)成像檢查,小視野成像系統(tǒng)則具有高空間分辨率,用于耳部?jī)?nèi)部機(jī)構(gòu)(中耳、內(nèi)耳)的成像檢查。
在此之前,醫(yī)院主要采用通用CT進(jìn)行耳部影像檢查,存在分辨率不足、關(guān)鍵結(jié)構(gòu)無(wú)法顯示、隱匿病變難以看清等不足。這一創(chuàng)新醫(yī)療器械的推出能夠有效解決通用CT對(duì)耳科精細(xì)解剖結(jié)構(gòu)成像不清的難題,從而推動(dòng)耳科疾病的基礎(chǔ)研究和臨床診療。
● 火速獲批的5.0T全身磁共振系統(tǒng)國(guó)際領(lǐng)先
該器械由上海聯(lián)影醫(yī)療科技股份有限公司推出,于2022年初獲批進(jìn)入創(chuàng)新醫(yī)療器械程序,核心技術(shù)“擁有自主知識(shí)產(chǎn)權(quán),關(guān)鍵性能指標(biāo)已達(dá)到國(guó)際領(lǐng)先水平”(NMPA評(píng)價(jià)),并于2022年8月火速獲批,整個(gè)審批流程不足一年,在創(chuàng)新醫(yī)療器械中實(shí)屬罕見(jiàn)。
基于3.0T的時(shí)間飛躍磁共振血管成像能夠清晰顯示腦血管結(jié)構(gòu),是目前臨床一線的無(wú)創(chuàng)腦血管成像技術(shù)。但其抑制背景組織信號(hào)不佳,對(duì)大血管遠(yuǎn)端分支和細(xì)小穿支動(dòng)脈的評(píng)估無(wú)法滿足臨床需求。超高場(chǎng)強(qiáng)7.0T技術(shù)可以解決這一短板,但場(chǎng)強(qiáng)的提升會(huì)使得B1場(chǎng)的不均一性和受試者生理不適感增加。
5.0T磁共振系統(tǒng)則實(shí)現(xiàn)了平衡,首次突破了超高場(chǎng)磁共振局限于腦部成像的限制,可實(shí)現(xiàn)超高場(chǎng)全身臨床成像;在神經(jīng)系統(tǒng)成像方面更是比肩更高場(chǎng)設(shè)備,可為腦小血管疾病與退行性病變提供更多診斷信息。
對(duì)比先進(jìn)水平,我國(guó)醫(yī)療器械創(chuàng)新發(fā)展空間巨大
從兩國(guó)創(chuàng)新醫(yī)療器械審批不難看出,我國(guó)醫(yī)療器械創(chuàng)新較全球先進(jìn)水平仍有提高空間,但近年來(lái)發(fā)展勢(shì)頭迅猛也是不爭(zhēng)的事實(shí)。
對(duì)比FDA的突破性設(shè)備和NMPA的創(chuàng)新醫(yī)療器械審批,F(xiàn)DA的風(fēng)格更偏向于“寬進(jìn)嚴(yán)出”。盡管歷年納入名單的器械數(shù)量十分龐大,但最終拿到上市申請(qǐng)的占比僅有8.9%。
相比之下,我國(guó)創(chuàng)新醫(yī)療器械審批則有所不同。根據(jù)歷年情況匯總統(tǒng)計(jì),在獲準(zhǔn)進(jìn)入創(chuàng)新醫(yī)療器械程序這一步的通過(guò)比例約為21%,但在進(jìn)入創(chuàng)新醫(yī)療器械審批程序后成功拿到醫(yī)療器械證的比例則高達(dá)51%。如果再加上各地方局的2類創(chuàng)新醫(yī)療器械,通過(guò)率或許會(huì)更高。
不過(guò),考慮到我國(guó)創(chuàng)新醫(yī)療器械目前還處于國(guó)產(chǎn)替代、微創(chuàng)新和跟隨式創(chuàng)新階段,這種情況也實(shí)屬正常。
值得一提的是,我國(guó)創(chuàng)新醫(yī)療器械的同質(zhì)化程度明顯較高。以2022年進(jìn)入創(chuàng)新醫(yī)療器械通道的產(chǎn)品為例,心血管類創(chuàng)新醫(yī)療器械為第一大類,占比超過(guò)一半。相比之下,心血管類器械雖然也是“突破性設(shè)備”第一大類,但所占比例遠(yuǎn)不一樣。
此外,在2022年,手術(shù)機(jī)器人進(jìn)入創(chuàng)新醫(yī)療器械名單的數(shù)量?jī)H次于心血管,但這些產(chǎn)品是否都能夠滿足臨床需求,或許也需要進(jìn)一步觀察。
這一現(xiàn)象的背后,也折射出我國(guó)醫(yī)療器械創(chuàng)新與全球頂尖水平的差距,包括在研發(fā)的投入、科研轉(zhuǎn)化、基礎(chǔ)科學(xué)的加強(qiáng)乃至后續(xù)的進(jìn)一步產(chǎn)品化和商業(yè)化上。我國(guó)醫(yī)療器械創(chuàng)新仍然有相當(dāng)長(zhǎng)的路要走。
好消息是,基于巨大的需求,國(guó)家對(duì)醫(yī)療器械創(chuàng)新愈發(fā)重視,醫(yī)療新基建浪潮持續(xù)落地對(duì)于國(guó)產(chǎn)龍頭企業(yè)也是巨大利好。同時(shí),政策有意扶持,國(guó)產(chǎn)替代和醫(yī)保支付對(duì)創(chuàng)新醫(yī)療技術(shù)都給予了一定的優(yōu)惠,使得創(chuàng)新成果有機(jī)會(huì)在更短時(shí)間實(shí)現(xiàn)商業(yè)價(jià)值,從而快速成長(zhǎng)。此外,背靠我國(guó)強(qiáng)大制造業(yè)基礎(chǔ),醫(yī)療器械創(chuàng)新也有較好的發(fā)展基礎(chǔ)。
我們相信,國(guó)內(nèi)醫(yī)療器械創(chuàng)新在未來(lái)必然會(huì)呈現(xiàn)更好的發(fā)展,也終將會(huì)在全球版圖中占據(jù)重要的地位。



