文|i美妝頭條 姚立凡
編輯|黃友枝
1月28日,國家藥監局發布公告稱,YY/T 1888-2023《重組人源化膠原蛋白》醫療器械行業標準已審核通過,并將于2023年7月20日實施。該標準規定了重組人源化膠原蛋白的質量控制、技術要求、試驗方法、穩定性、生物學評價以及包裝、運輸和貯存等。
另外,2023年1月29日,國家藥品監督管理局醫療器械標準管理中心發布了《重組膠原蛋白生物材料命名指導原則》解讀,以更好地指導和規范重組膠原蛋白醫療器械的命名工作。

兩則重組膠原蛋白文件的發布,不僅傳遞出國家層面對于重組膠原蛋白在醫療、護膚等行業應用的認可,也將為重組膠原蛋白行業帶來更加規范化、標準化發展的引導。
01、重組膠原蛋白異軍突起
從動物源膠原蛋白到重組膠原蛋白,在科研力量的驅動下,膠原蛋白行業迎來新的突破與發展,重組膠原蛋白成為更優質、更有應用發展前景的新型膠原蛋白材料。化妝品市場的聚光燈也再次投向了重組膠原蛋白這條潛在的高景氣賽道。
眾所周知,膠原蛋白(Collagen)作為一種功效蛋白質,在化妝品中起到抗皺、修護皮膚屏障、保濕等作用,在美容護膚和大健康領域都備受關注。哈佛醫學院麻省總醫院皮膚生物學研究中心研究員陳宏翔教授就曾公開表示,皮膚的衰老本質就是膠原蛋白的流失,在皮膚中I型膠原蛋白占85%,Ⅲ型膠原蛋白占比10%-15%,膠原蛋白的補充對于延緩皮膚衰老有著至關重要的作用。
而以往的膠原蛋白來源主要是以動物源為主,存在著潛在的排異風險和病毒隱患。隨著合成生物學的發展與進步,膠原蛋白在基因重組技術上的突破,重組膠原蛋白問世,成為更優質、更有應用發展前景的新型膠原蛋白材料。
資料顯示,重組膠原蛋白是利用DNA重組技術制備的膠原蛋白,其氨基酸序列可根據需求進行設計改進,如重組人源化膠原蛋白的重復單元與人膠原蛋白氨基酸序列特定功能區相同。這種制備方式可實現定制化合成,即不僅可合成不同類型的膠原,還可篩選出不同型別膠原分子上的特定功能區并根據需要進行定制組合。
由于重組膠原蛋白的序列與人體的基因序列高度一致,組織相容性較好,可以被人體直接吸收并參與構建膠原蛋白,具有生物活性及生物相容性更高、免疫原性更低、病原體隱患風險更低、水溶性更佳、無細胞毒性、可進一步加工優化以及更容易運輸和儲存等多種優勢。截至目前,國際上已有230余項臨床研究和學術文獻證明重組膠原蛋白的優秀性能。
巨子生物研發總監王小軍告訴美妝頭條,伴隨著生物科技的迅速發展,尤其是國內重組膠原蛋白產業化和應用研究已經達到國際領先水平,現有研究結果證實重組膠原蛋白安全性高、生物學功效確切,是能夠應用于多個領域的生物活性成分,加之消費者消費升級,對于產品的安全性和有效性均提出了更高要求,因此重組膠原蛋白備受追捧。
在他看來,隨著越來越多以重組膠原蛋白為原料的產品推出并在市場上贏得良好口碑,重組膠原蛋白將迎來高速發展的黃金時期。
弗若斯特沙利文數據預測,2022-2027年,我國重組膠原蛋白產品的市場規模將以42.4%的復合年增長率從185億元增至1083億元,高于動物源膠原蛋白25.3%的增速。
02、市場規范化,重組膠原蛋白行業標準出爐
伴隨著重組膠原蛋白賽道入局者越來越多,難免會有虛假宣稱、概念添加等泥沙俱下的亂象。為進一步規范膠原蛋白市場,國家藥監局先后頒布了多項行業標準及政策,分別對重組膠原蛋白生物材料命名、產品監督管理及質量控制等作出規范要求。
例如,目前市場上存在重組膠原蛋白宣傳不規范的行為,比如使用“全人源重組膠原蛋白”、“去端重組膠原蛋白”以及“類人(源)重組膠原蛋白”等不規范用語。
為解決行業存在的不規范用語現象,2021年3月,國家藥監局發布的《重組膠原蛋白生物材料命名指導原則》提到,重組膠原蛋白生物材料名稱由核心詞和特征詞組成,按“特征詞(如有)+核心詞(A+B)”結構編制。
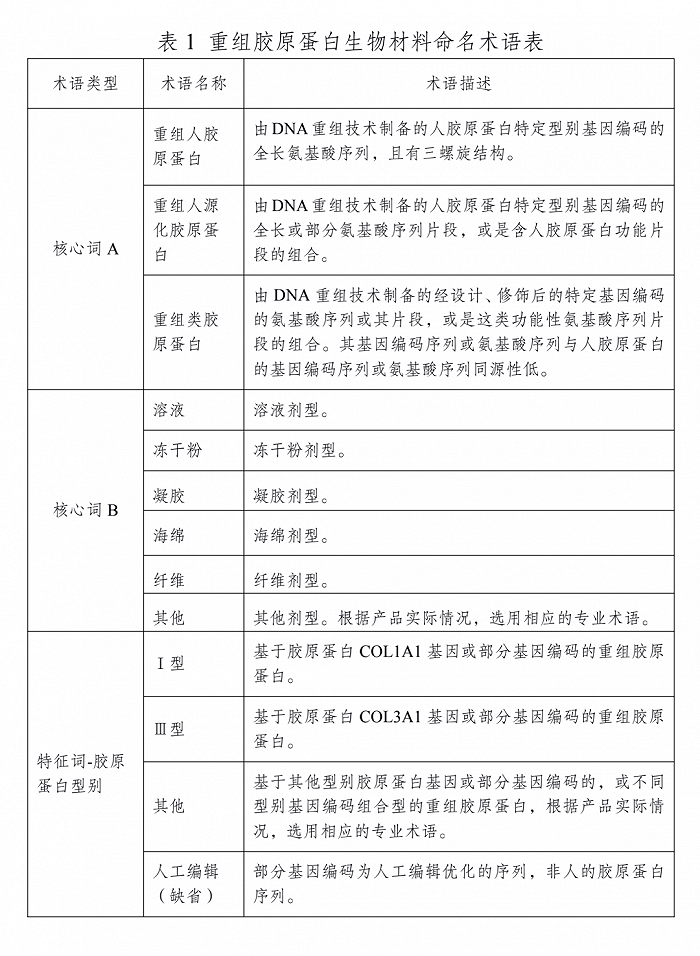
根據《指導原則》,A項核心詞只有3個,包括“重組人膠原蛋白”“重組人源化膠原蛋白”“重組類膠原蛋白”。B項核心詞包括:溶液、凍干粉、凝膠、海綿、纖維、其他。特征詞則有Ⅰ型、Ⅲ型、其他。
值得一提的是,2023年1月29日,國家藥品監督管理局醫療器械標準管理中心發布了《重組膠原蛋白生物材料命名指導原則》解讀,以更好地指導和規范重組膠原蛋白醫療器械的命名工作。

重源品牌市場經理凌詩雅坦言道:“重組膠原蛋白行業是新興行業,很熱鬧,也很不規范,甚至很多業內人士對于重組膠原的命名規則都不甚了解,尤其是目前重組膠原大量被應用在醫美領域,這事關消費者的生命安全和整個行業的發展前景,所以相關部門盡早介入,持續更新行業標準,也是為了更好地規范亂象。”
她認為,重組膠原蛋白行業標準的建立和實施,代表了國家層面對于重組膠原蛋白在醫療、護膚等行業應用的認可,行業標準的出爐從初期也能夠幫助真正做科研、搞技術、符合安全標準的企業走得更長久,整個行業發展得更健康。
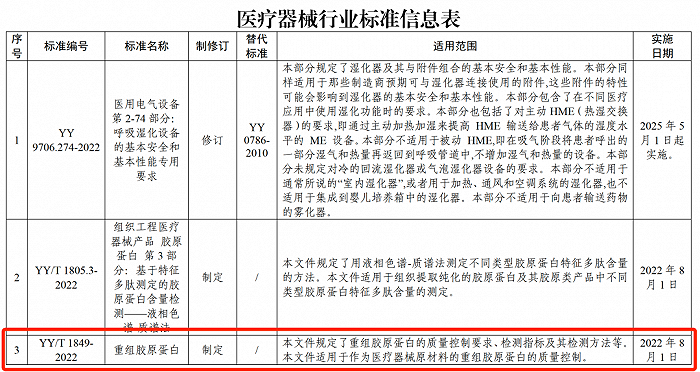
為進一步規范膠原蛋白市場,2022年1月13日,國家藥品監督管理局發布了《重組膠原蛋白》(YY/T 1849-2022)行業標準,并已于2022年8月1日正式實施。該標準規定了重組膠原蛋白的質量控制要求、檢測指標及其檢測方法等,適用于作為醫療器械原材料的重組膠原蛋白的質量控制。
這份文件的發布,是國家首次針對重組膠原蛋白在醫藥領域出臺的行業標準,既代表了國家層面對于重組膠原蛋白在醫療、護膚等行業應用的認可,也將在很大程度上引導重組膠原蛋白的規范化、標準化發展。
2022年4月,國家藥監局綜合司發布關于《重組人源化膠原蛋白》醫療器械行業標準立項的通知,行業標準制定的主要出發點是為鼓勵重組人源化膠原蛋白新型生物材料研發創新,推動醫療器械產業高質量發展。
2023年1月28日,國家藥監局發布公告稱,YY/T 1888-2023《重組人源化膠原蛋白》醫療器械行業標準目前已審核通過,并將于2023年7月20日實施。此次新規發布也將為行業帶來更加正向的引導。
“新出臺的標準還是基于《重組膠原蛋白》的行業標準,基本內容一致,是對于重組人源化膠原蛋白做為醫療器械原材料的質量要求進行了細化要求。”王小軍認為,未來還會有針對化妝品甚至是食品的重組膠原蛋白相關標準出臺,這反映了國內企業對于重組膠原蛋白的開發研究進入了快車道,應用場景也會越來越多,行業發展趨于規范,門檻變高,對于頭部企業的發展是重大利好。
03、重組賽道白熱化,資本與企業急速狂飆
此次行業標準的正式實施,膠原蛋白行業越來越規范化的同時,競爭也越發激烈,前有巨子生物、錦波生物、創爾生物,后有華熙生物、江蘇吳中等紛紛入局,資生堂在中國的首投也選擇了中國膠原蛋白企業創健醫療,持續擴大的膠原蛋白賽道,不斷地上演著風起云涌地較量和爭奪。
港交所上市的巨子生物,早在2000年,在全球范圍內率先實現重組膠原蛋白科研成果轉化及產業化,也是全球范圍內擁有最大重組膠原蛋白產能的企業之一。據巨子生物的招股書顯示,其2021年重組膠原蛋白產能達到10.9噸,并計劃于2023年擴展超過200噸。目前巨子生物自主研發的多款基于重組膠原蛋白的Ⅲ類醫療器械產品已進入臨床試驗階段。
與此同時,巨子生物已經構建起了一個重組膠原蛋白分子庫,“分子庫”中已儲備的33種不同類型的重組膠原蛋白,包括3種全長Ⅰ、Ⅱ、Ⅲ型重組膠原蛋白,5種重組膠原蛋白功效片段,25種功能強化型重組膠原蛋白。
頭部玩家錦波生物則通過對天然人源膠原蛋白序列進行重復拼接,開發了一種基于III型膠原蛋白的重組人源化膠原蛋白。自主研發的三類醫療器械“重組Ⅲ型人源化膠原蛋白凍干纖維”與其核心品牌“薇旖美”于2021年6月獲得國家藥監局批準上市,是國內唯一獲批的可注射重組人源化膠原蛋白產品。
透明質酸巨頭華熙生物在2022年年底表示,其近年加大投入合成生物,膠原蛋白項目年底可以實現化妝品級的量產,并將膠原蛋白視為繼透明質酸之后的第二大戰略性生物活性物。目前,華熙生物在膠原蛋白領域已全線布局重組人源膠原蛋白、動物源膠原蛋白、水解膠原蛋白(肽)三大細分領域。
老牌美妝企業丸美股份攜手暨南大學基因工程研究院,推出美麗法則與丸美膠原蛋白次拋等新型產品。值得一提的是,丸美股份舉辦第二屆重組膠原蛋白抗衰老論壇,發布一系列重組膠原蛋白研究成果,將持續投入億元資金,展開對重組膠原蛋白未來長達十年的研究。
此外,在其他潛在玩家中,暨源生物同樣在布局重組人源化膠原蛋白、重組類人膠原蛋白的研發生產;國際化妝品巨頭資生堂也在2022年投資了專注于重組膠原蛋白研發的創健醫療,加速推進重組膠原蛋白生物材料創新發展……
重組膠原蛋白賽道火熱異常的同時,我們也要看到,目前重組膠原蛋白市場仍處于技術成本高,產業化規模仍較低的局面,重組膠原蛋白可量產和應用的種類還不夠多,多種類型重組膠原蛋白的生物活性和作用機理等還有待進一步深入研究。
暨南大學教授熊盛就曾公開表示:“生產制造難,結構設計、功能仿生難,生物學活性表征難,行業標準不規范等都是這一領域不容忽視的問題。”并直言,生產成本是重組膠原蛋白領域不得不面對的難題。不同于玻尿酸,目前重組膠原蛋白生產成本依然居高不下,產業化規模仍有待持續擴大,市場期待活性更強、性價比更高的重組膠原蛋白的廣泛應用。
有業內人士透露,60%-90%純度的重組膠原蛋白,價格在每公斤十幾萬以上,純度100%膠原蛋白市場價格可能去到每公斤超百萬元。
此外,教育成本高,接受門檻高也是重組膠原蛋白現階段需要解決的難題。凌詩雅表示,重組膠原蛋白需要教育和科普的內容相當多,短時間很難觸達消費者的認知。另外重組人源化膠原蛋白它不是填充材料,而是再生材料,短時間內很難讓消費者快速看到變化,同時也因為技術門檻高,價格相應也會比較高,所以很難快速擊穿消費者決策。
那么,作為下一個能支撐起某個產業規模化增長的熱門原料成分,重組膠原蛋白又該如何突破技術成本高,產業化規模仍較低的局面呢?
在王小軍看來,重組膠原蛋白發展需要從橫縱兩大方向進行突破。首先是橫向,要求研發人員開發出更多種類型具有不同功能的重組膠原蛋白并產業化,同時根據新型重組膠原蛋白的功能和分子量等特性應用于不同領域,進一步拓展其應用場景。
他表示,由于不同類型的重組膠原蛋白的生產難度差異較大,比如全長α鏈的生產就比片段型或拼接型難度大很多,所以具有先行優勢和投入更多研發力量的企業將會贏得先機。
第二是縱向,對于每一種重組膠原蛋白的功效進行驗證并深入研究其作用機制,為各類產品的開發提供理論依據,為企業筑起了一道堅固的“護城河”。
正是由于還有更多需要攻關的技術瓶頸,重組膠原蛋白市場方興未艾,才能激發更多的資本與企業去掘金,更深入地布局這一賽道。可以肯定的是,借助新標準、新政策、新方向,重組膠原蛋白市場的發展將迎來一個新的時代。
監制 | 陳山花


