文 | 財健道 吳妮
編輯 | 楊中旭
5月24日開盤,君實生物(688180.SH/01877.HK)在A股和港股的股價雙雙跳水,A股一度觸及跌停,港股現跌超12%。
難以想象,君實的大跌源于一個“好消息”——5月23日晚間,君實生物發布《上海君實生物醫藥科技股份有限公司關于 VV116 對比 PAXLOVID 早期治療輕中度COVID-19的III期注冊臨床研究達到主要研究終點的公告》(以下簡稱“公告”),稱其與旺山旺水合作開發的新冠口服藥VV116,在一項對比輝瑞口服藥PAXLOVID用于輕中度新冠早期治療的III期注冊臨床研究(NCT05341609)上,達到方案預設的主要終點。

關注新冠口服藥的人可能還記得,4月6日開拓藥業(09939.HK)公布普克魯胺“相應保護率為100%”,當日股價上漲106.37%的盛況。那為何君實公布III期臨床成功的結果后,會被資本的巨浪拍在沙灘上呢?
浩悅資本資深合伙人李逸石表示,股市會對此前公開和甚至不公開的消息進行預期和計價(price in),如果企業的新動向沒有達到預期,市場就會以下跌作為反饋。
如果沒有官宣,市場就還持有更好的預期;一旦官宣,意味著預期破滅。而股價是預期的折現。
目前國產新冠口服藥處于沖刺階段的有三家,真實生物的阿茲夫定、開拓藥業的普克魯胺以及君實生物的VV116。對于三者之中誰會最先撞線的問題,一直爭論不斷。而這次《公告》給君實的支持者澆了一盆冷水。
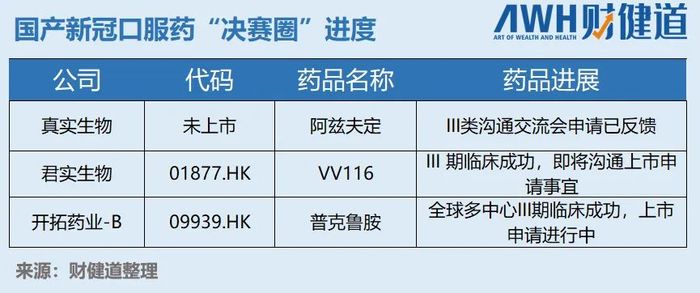
君實在《公告》中表明公司將于近期與監管部門溝通遞交新藥上市申請事宜,結合NMPA公開信息,可以得知君實才進展到II類會議,且尚未得到反饋。
開溝通交流會意味著什么?
國家藥監局藥品審評中心于2020年12月10日發布了《藥物研發與技術審評溝通交流管理辦法》。在該辦法中,對溝通交流進行了定義,即溝通交流是指在藥物研發與注冊申請技術審評過程中,申請人與藥審中心審評團隊就現行藥物研發與評價指南不能涵蓋的關鍵技術等問題所進行的溝通交流。其中,溝通交流會議根據不同的情況分為Ⅰ類、Ⅱ類和Ⅲ類會議。
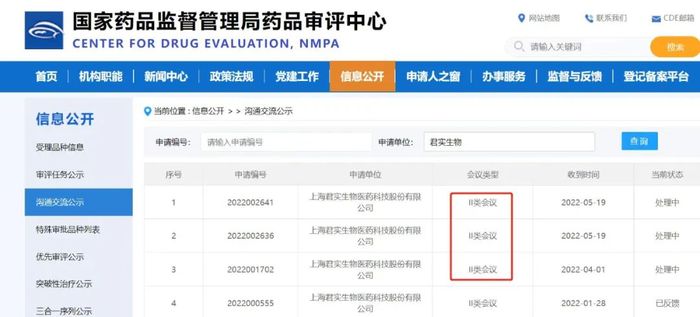
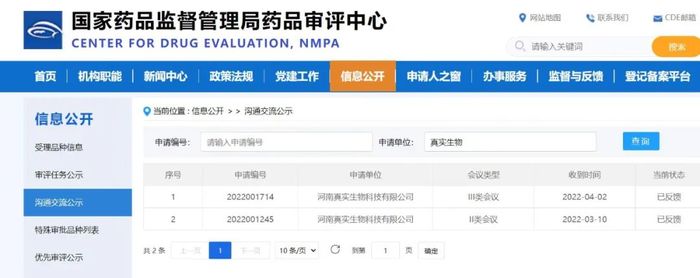
雖然君實新藥作為新藥,可能不需要III類會議,但依然被真實生物拉開了一個多月的進度。
真實生物早于4月2日得到了III類會議的反饋。再加上,真實生物為阿茲夫定接連簽下三家生產經銷商,“首個國產抗病毒阿茲夫定即將在平頂山投產”等消息釋出,讓阿茲夫定看起來已經沖刺在即了。
來自開拓藥業的壓力也不小。開拓藥業負責人日前證實,國家藥監局正在審理普克魯胺新冠適應癥的上市申請。
如果說,君實在審批速度上有什么優勢的話,可能是與輝瑞Paxlovid的頭對頭試驗。頭對頭試驗可以直接檢驗藥效, 對審核有巨大推動作用。
在業內人士劉超看來,對新冠口服藥這種戰略型產品來說,在輝瑞Paxlovid引入中國市場后,相應地,國內審批至少會再批準3家新冠口服藥。所以說三者的勝負不能根據速度下定論,療效和安全才是最重要的。
那么問題又來了,VV116能夠憑借有效性和安全性反超嗎?
本次《公告》臨床研究結果顯示,VV116用于輕中度COVID-19的早期治療達到臨床方案預設的主終點。然而,君實選取的主要終點,并非CDE的指導原則下最優的評價——降低重型/危重型和死亡發生率指標,而是“至持續臨床恢復的時間”——即受試者的新冠病毒轉陰時間。
《公告》里沒有披露臨床數據,但5月17日,君實在Emerging Microbes &Infections 期刊上曾初步評價了輕癥奧密克戎感染患者核酸轉陰這單一指標。研究數據提示,在首次核酸檢測陽性5日內使用VV116的奧密克戎感染患者,其核酸轉陰時間為8.56天,小于對照組的11.13天。
在新藥研發從業者周葉斌博士看來,這個數據遠遠不夠。核酸轉陰時間縮短反應的是載毒量下降更快,但抗病毒藥更關鍵的是對疾病的治療作用,比如轉重癥的比例是否下降。而且,降低重癥風險也是輝瑞口服藥在臨床試驗里體現出來的作用,要與輝瑞口服藥比較非劣性,也要從這一點出發。
君實這波屬于田忌賽馬了。
業內對于VV116的其他質疑也都與臨床數據相關。《公告》里提出的次要研究終點,即重癥改善情況,被市場普遍認為是VV116獲批上市的關鍵。VV116能否達到這一研究終點?國際多中心臨床研究數據又如何?
歷史總是驚人的相似。開拓藥業于4月6日公布臨床III期試驗關鍵數據時,也飽受爭議。公告中,相比此前更常見的治愈率、致死率、阻斷率等等,開拓藥業更多地使用“保護率”這一詞。業內人指出,開拓藥業可以自行定義“保護率”這個詞的用法,但通常來說,還是要去跟國際藥廠或者現有新冠口服藥做頭對頭的對比,從減少危重癥,減少住院或死亡率等常規數據角度進行比較。100%這一數據也讓醫學界、投資界為之警覺。
對于君實與開拓來說,最好的回應,是更多的臨床數據和真實世界的驗證。
上下游產業早已摩拳擦掌,疫情中的人們也翹首以盼,希望國產口服藥能夠不負眾望。
(作者系《財經》研究員)
制圖 | 李紫雅
參考文獻
【1】市場關注普克魯胺熱度不減 開拓藥業回應股東權益變動披露.投研電訊.2022.5.20
【2】最新解讀:從君實V116公告看國產新冠藥的真實進度!.財經星星眼.2022.5.24
【3】21醫政解讀|助推藥企真創新力度再升級,CDE新政為突破性治療藥物審評加速度.21世紀經濟報道.季媛媛.2022.2.24
【4】最新研究!我國研發的這款口服抗新冠藥物,對部分非重癥奧密克戎感染患者,或能縮短核酸轉陰時間.每日經濟新聞.2022.5.18


