文|IT時報記者 郝俊慧
編輯|挨踢妹
2月15日,藥明康德發布業績快報,2021年營業收入為229.02億元,同比增長38.5%;歸母凈利潤50.97億元,同比增長72.19%。靚麗的數據給藥明康德的股價打了一劑強心針,春節過后,藥明康德再次暴跌,一路下探至2月11日的81.9元,隨后受益于良好的業績曾略有回升,今日股價報收96.80元,但距離其2021年中高位的170元左右,仍有超四成的跌幅。
藥明康德的疲態,“拖累”了明星基金經理——中歐基金的葛蘭,天天基金顯示,重倉藥明康德、凱萊英、康龍化成等CXO(醫藥外包)企業的中歐醫療健康混合A基金近一年回撤34.6%。
冰火兩重天。與這些在二級市場“閃崩”的醫藥股相反,生物醫藥的另一個賽道——AI制藥,卻在2021年收獲了一級市場投資人的熱情。據動脈網不完全統計,2021年,國內AI制藥領域共發生34起融資事件,融資總額約為83.45億元。其中僅晶泰科技一家便在去年8月完成4億美元(約等于25.3億人民幣)D輪融資,估值超過130億人民幣,此時,距離晶泰上次3億美元的C輪融資還不到1年。
4年前,《我不是藥神》揭露了一個令人心酸的事實:高昂的研發成本,只能轉換為罕見病患者不得不承擔的藥價。彼時正是人工智能產業化的開始,《IT時報》記者調查顯示,利用AI輔助的First-in-class(首創新藥),國內投資界和藥企并不十分積極,Me-too新藥顯然能更快帶來短期收益。但隨著技術進步以及2021年一系列政策推出,研發周期可能縮短至平均5年,成功概率最高可突破45%的AI制藥,將真正走上醫治人類病痛的舞臺。
01 AI制藥進入臨床階段

盡管還沒有一家AI制藥企業的產品通過FDA(美國食品和藥物管理局)批準上市,但已經有藥物被批準進入臨床研究(IND),這被認為是AI制藥價值閉環的重要驗證。
2021年年底,國內人工智能制藥公司Accutar Biotechnology(冰洲石生物科技)宣布,用于治療轉移性去勢抵抗性前列腺癌的AC0176研究性新藥獲批進入IND,這是三個月內Accutar第二個獲批進入臨床的藥物。從Accutar 宣布的消息中可知,從AI藥物發現平臺到藥理驗證平臺的閉環實踐,是其在兩年短周期內完成,這是一個被認為價值數十億美元的研發過程。
相較于傳統創新藥研發流程,這個速度不可思議。
藥企往往用“三十定律”來解釋昂貴的藥價:10億美元的投入、10年的研發周期和低于10%的成功率,尤其是罕見病藥物,正版藥幾無降價空間。AI輔助制藥則被看作可以通過深度學習,在靶點發現與驗證、分子發現與優化等環節大幅提高研發效率。
一個具有劃時代意義的技術突破發生在2021年7月,AlphaFold 2公開了其預測的人類和其他20種重要物種的蛋白質組所有結構,這意味著,藥物研發不再強烈依賴于實驗組解析的晶體。由于每個蛋白都可能是某種疾病的靶點,科學家們可以針對每個蛋白設計出對應的分子進行調控,更好地預判蛋白質與分子結合的概率,從而加速新藥研發。
藥企向AI制藥拋出的訂單也越來越“誘人”。今年1月,藥企巨頭賽諾菲與AI制藥公司Exscientia共同宣布,合作開發多達15種腫瘤和免疫學領域的候選藥物,交易金額高達52億美元。根據協議,如果賽諾菲將合作產品商業化,Exscientia將獲得最高21%的銷售分成。
“新藥研發設計環節多、周期長,不同場景所需要的技術架構和專業知識也不一樣,大多數初創企業都是選擇一兩個細分領域進入,但Exscientia可以為賽諾菲開發15條管線(藥物品類),一方面顯示了自己的技術實力,同時也從側面說明,AI輔助制藥的能力在加強。”一位醫藥投資界人士向《IT時報》記者解釋。
從2020年1月第一款AI研發的新藥候補化學物進入第一段臨床開始,截至2021年7月,據中信證券不完全統計,AI主導、進入臨床階段的管線已經超過20余項。臨床階段通常需3-6年時間,據于此,最快在2023年,可能會有AI藥物進入審批環節。更樂觀的設想是,到2025年,或許第一款AI藥物會進入生產上市流程。
02 內卷的Me-too創新藥
2018年7月,《IT時報》曾在《十年八載,AI打算研發一款抗癌新藥》中提及,我國藥物研發基礎較為薄弱,創新藥以Follow—on(隨式)創新藥為主,而AI輔助的First-In-Class(首創新藥)的藥物研發企業,則在資本層面存在不同態度。時隔3年多,風向逆轉。
中國的生物醫藥賽道起步于2015年,隨著國家醫改拉開大幕,醫藥健康產業被定位為國民經濟的“支柱行業”,創新藥物的研發作為醫療行業上游產業鏈的核心領域,成為資本市場角逐的重點。
然而,盡管每年國產創新藥獲批的數量都在增加,屬于First-In-Class(FIC)的并不多。
所謂Follow—on(跟隨式)或者Fast-Follow(快速追蹤)模式,是指不侵犯他人專利的情況下,在已有靶點和機理的基礎上,對新藥進行分子結構改造或修飾,尋找作用機制相同或相似,具有新治療效果的新藥物,包括Me-too、Me-better、Me-worse等藥物。
換而言之,Fast-Follow(快速追蹤)是“站在巨人肩膀上的創新”,但問題是,站在“肩膀”上的企業,太多了。
國家藥品監督管理局藥品審評中心(CDE)2021年11月發布的《中國新藥注冊臨床試驗現狀年度報告(2020年)》顯示,臨床試驗數量最多的前10位靶點依然是PD-1、 VEGFR 等耳熟能詳的靶點,其中PD-1(抗腫瘤治療的靶點)更是有75個藥物品種申請登記臨床試驗。
“太卷了”。對于過去兩年的國產創新藥研發,多名醫藥行業人士都表示,同質化競爭嚴重。
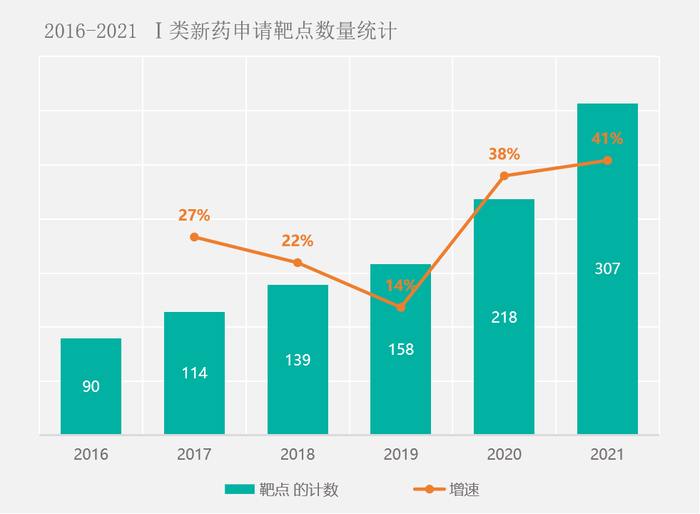
《中國I類新藥靶點白皮書》顯示:2016-2021年,我國I類新藥申請受理數量逐年提高,年復合增長率(CAGR)高達40%。然而,前6%的靶點便已囊括了超40%的新藥,其中國內僅申報并獲CDE受理的PD-L1新藥就近60款,而國內的PD-L1新藥大量都是Fast-Follow。
2022年1月,美國FDA藥物評價和研究中心(CDER)發布了《2021年度的新藥獲批報告》,這一年里,美國FDA一共批準了50款新藥,其中27款為“first-in-class”療法,占全年獲批新藥總數的54%,占比為10年最高。
03 政策助推 站上風口
國產創新藥“扎堆”Fast-Follow的直接后果是,同質藥價格競爭激烈、利潤率下降,進而導致臨床資源浪費、資金浪費。于是,2021年下半年與市場“寒風”一起到來的,還有政策的“冬天”。
2021年11月19日,CDE六連發重要文件。其中,《以臨床價值為導向的抗腫瘤藥物臨床研發指導原則》(簡稱《指導原則》)明確提出,在藥物進行臨床對照試驗時,一是應盡量為受試者提供臨床實踐中最佳治療方式/藥物;二是新藥研發應以為患者提供更優的治療選擇為最高目標。這被解讀為,監管部門將遏制Me-too新藥的泛濫,尤其不支持Me-worse新藥。
從7月《指導原則》開始征求意見起,二級市場里的生物醫藥賽道便被戳破了泡沫,一路下滑至今,由于《指導原則》中有關臨床對照試驗選擇的BSC變化直接降低了Me-too藥物上市的可能性,從而減少CXO公司可獲得訂單數目,資本市場對其前景的擔憂導致發生股市“踩踏”。
不僅藥明康德等上市公司股價跌跌不休,2021年下半年上市的幾家生物醫藥企業甚至跌破發行價。
與此相反,上述投資人士告訴記者,2020年以來,AI制藥已經成為投資圈的香餑餑,融資項目數量幾乎翻倍,同時,今日頭條、騰訊、百度等互聯網巨頭都開始涉及AI制藥領域,發現平臺“云深制藥”,百度在2020年9月成立生命科學平臺“百圖生科”,“今后幾年,這種熱度只增不減,最明顯的趨勢是,AI+生物醫藥企業間的人才爭奪越來越厲害,薪資漲幅也屢創新高”。
BOSS直聘顯示,目前與AI制藥相關的主要崗位為生物信息工程師、算法工程師與AI制藥專家,生物工程師主要負責藥物研發與實驗,平均月薪為2.5萬元,AI制藥專家則是要求候選人同時具備生物制藥與機器算法的專業能力,學歷與工作經歷要求比生物工程師與算法工程師更高,平均月薪3.5萬元。2020年底,字節跳動招聘生物信息工程師,月薪也開到了4萬元左右。
如果是頂尖人才,百萬美元年薪也不鮮見。百度旗下的生命科學公司百圖生科便開出100萬美元的天價年薪招聘首席科學家。
04 買單者越來越多
今年1月,上海復星醫藥與英矽智能宣布合作,在全球范圍內共同推進多個靶點的AI醫藥研發。根據協議,英矽智能獲得1300萬美元的首付款以及里程碑式付款,并分享QPCTL項目商業化的利潤。這是國內迄今為止AI制藥企業收到的最大額預付款。
盡管合作金額與賽諾菲和Exscientia的協議相差甚遠,但對于國內AI制藥初創企業而言,這絕對是個好消息。前兩年,盡管資本對AI制藥熱情高漲,但國內藥企卻并沒有幾家拿出真金白銀來買單。
情況正在發生變化。晶泰科技CEO馬健此前接受雷鋒網采訪時回憶,2020年初,和藥企談合作時,他經常要介紹一些基本概念:AI制藥是什么,AI怎么跟藥物研發結合,但到了2021年,藥企開始追問更多細節:技術差異點是什么?使用了什么樣的技術?
“目前藥企和AI制藥公司應該在試水階段,早期研究到臨床階段的周期越來越短,藥企對于AI的作用認知越來越清晰。”上述人士透露,盡管像復星醫藥和英矽智能這樣的大單在國內還不多見,但愿意拿出部分研發方向給AI制藥公司試水的藥企越來越多,合作金額也在逐年上升。
2021年2月,英矽智能曾對外宣布,僅用了18個月、投入260萬美元,就研發出特發性肺纖維化疾病新靶點。德睿智藥則在今年1月17日宣布,用其自主研發的一體化AI新藥發現平臺Molecule Pro,在8個月時間內設計、驗證了69個全新的小分子并獲得了針對某B類G蛋白偶聯受體(Class B GPCR)靶點的臨床前候選化合物,目前該自研管線已進入IND-Enabling Studies階段。傳統研發過程中,這個階段至少5-8年,如今兩家AI制藥明星企業與國內藥企往來密切。
不過前方也并非一片坦途。盡管AI制藥大大降低了藥企的試錯成本,但相較于相對成熟的Fast-Follow創新藥,從頭開始顯然風險更大,藥企究竟愿意為此拿出多少研發成本,市場前景并不明朗。
此外,AI制藥企業大多是初創公司,創始人在AI技術方面或某個細分領域或許是頂尖人才,可面臨的挑戰是,缺少數據。無論是醫院還是藥企的數據,如果沒有良好的合作關系,都不可能向這些初創公司開放。同時,隨著大藥企近幾年自建AI團隊,年輕的公司將面臨更大的挑戰。
不過,可以看到的是,生物科技的“奇點”爆炸在即,AI制藥的時代終將到來,讓天下沒有難做的藥,或許并不只是夢想。
排版/朱唯



