文|動脈網
今年5月,安徽醫科大學第一附屬醫院和云南農業大學合作,成功將經過基因改造的豬肝臟移植到了一位肝癌重癥患者身上。
術后第七天,患者已能下地自由活動,沒有發現超急性和急性排斥反應,凝血系統無障礙,肝功能已恢復正常。移植豬肝方面,每天有200ml左右金黃色膽汁分泌,CT和B超證實移植豬肝臟肝動脈、門靜脈、肝靜脈血流完全正常。
這是全球第五起活體異種器官移植,僅2024年便發生了其中的三起。
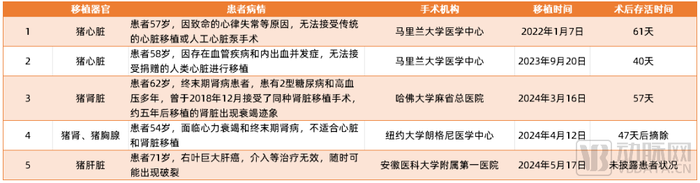
2022—2024年發生的5起活體異體器官移植
活體實驗外,死亡人體相關的移植試驗也在加速進行。今年3月,空軍軍醫大學西京醫院團隊將多基因編輯豬的全肝與腎臟分別移植到了兩位腦死亡人體內,術后均在一定時間內實現正常運轉。昆明醫科大學第一附屬醫院同樣找到了云南農業大學,開展了一起從豬到腦死亡人體的肝腎聯合異種移植實驗,同樣取得了不錯的進展。
爆發的臨床試驗之下,器官移植似乎已經走到了技術遷躍的邊緣。
如何補足超200萬的器官移植缺?
廣義上的器官移植不局限于動物到人體的移植,還包括技術已經相對成熟的人到人體,即將有活力的供體器官通過手術轉移至患者體內,以替代已經喪失功能的器官。
目前,我們的大部分器官已能實現移植,如心臟、肺、肝、腎臟、胰、小腸、皮膚等。此外,角膜和血管等組織的移植也已在臨床中廣泛應用。
不過,當下的器官移植產業遠談不上成熟。以最為常見的“換腎”為例,當雙側腎臟功能均喪失時,或是慢性腎功能不全發展至終末期,腎臟移植都是可行情況下的首選治療方案。此外,相比腹膜、血液透析,腎移植在長期存活率、生存質量和治療成本等方面均有明顯優勢。
但由于腎移植主要是通過配型的方法來進行,匱乏的腎源與不成功的配型下,很多患者直到病逝也未能等到治療機會。
參考國際器官捐獻與移植注冊數據,2020年底有超過34.54萬名患者仍在等待器官移植,僅在公布數據的那一年,等候名單中便有23103名患者,因未等到腎源遺憾去世。
還有一組數據能夠更為直接地闡述現狀:全球有逾266萬名接受透析治療的終末期腎病患者,僅有5.65%患者能夠獲得腎臟移植。
應對這一挑戰,全球各地都在推動產業相關法律法規的完善,建立更加透明、公正的器官捐獻移植體系,通過理順關系、明晰法律、加速傳播等樹立公眾對于器官移植的正常認知,進而鼓勵更多人群參與到器官的傳遞中。
譬如,西班牙、法國等每百萬人口器官捐獻率排名靠前的國家推行的是“默認同意”,即生前未明確表示拒絕捐獻者均被推定為器官捐獻者;美國大部分州采用了領取駕照時登記捐獻器官意愿的制度。
而在國內,國務院發布的《人體器官捐獻和移植條例》于今年5月1日正式施行,進一步對于器官移植行業進行規范。相比2007年施行的《人體器官移植條例》,新條例增加“捐獻”二字,凸顯器官捐獻的重要性,強化了對器官捐獻的激勵與引導。
與此同時,器官移植產業也在不斷進化,盡可能提高離體器官的存活率。
目前,主流的肝臟保存、轉運的機械灌注分為常溫灌注與低溫灌注兩種技術路徑,可服務于不同的供體和治療場景。
肝臟常溫機械灌注(NMP)的灌注溫度維持在35-38℃,器官處于生理代謝狀態,耗氧量大,灌注需使用氧合的血液制品。優勢在于可以通過膽汁生成和乳酸清除率來評估肝臟質量,作為平臺未來有治療遞送的應用空間;缺點在于短暫灌注中止也會造成肝臟二次缺血、血制品相關風險、操作復雜、灌注成本高。
肝臟低溫機械灌注(HMP)的灌注溫度維持在0-12℃,低溫狀態下肝臟代謝受抑制。優勢在于低溫下肝臟對缺血的耐受度更高,缺血造成的術后膽道并發癥率降低,且短暫的技術故障不會導致器官熱缺血損傷、造成功能丟失;缺點在于低溫下肝臟功能評估指標較NMP少。
在全球已實現商業化的肝臟機械灌注設備中,Transmedics與OrganOx兩家企業均應用NMP技術,XVIVO則采用可調溫灌注系統。國內的健耕醫療、奇點醫療、萊普晟的機械灌注均采用HMP技術。
其中,健耕醫療的 LifePort腎臟灌注運轉箱被近 40 個國家和地區、數百家 OPO 或移植中心使用。美國 57 家 OPO 中的 54 家使用 LifePort的產品進行供腎機械灌注,市場占有率第一。

健耕醫療LifePort產品體系
奇點醫療則是與中山一院實現深度合作,推出了“無缺血肝臟灌注系統”,實現為離體器官供血供氧,在不中斷血流情況下維持肝臟正常生理功能,顛覆了傳統器官冰鮮保存方式,極大程度上避免了供體器官缺血再灌注損傷,顯著改善移植預后,將器官移植推向了“熱移植時代”。
此外,該企業還將技術突破直指腎源,推出“器官拯救者”設備。該設備可利用既往手段無法實施捐獻的器官——心死亡器官捐獻,有望增加50%以上的器官來源,緩解器官短缺問題。
異種移植,器官移植的終極路徑?
盡管圍繞離體器官存活率展開的各種創新有效提高了移植患者的五年生存率,亦在一定程度上擴展了可用活體器官的供應量。但要補足移植患者龐大的需求缺口,異種器官移植才是解決問題的根本之道。
在非人靈長類動物模型的臨床前研究中,腎臟和心臟被認為是最適合進行異種移植的器官。經CRISPR修飾該豬的基因組以敲除抗原編碼基因,并加入人類基因并清除豬病毒,該豬腎在試驗猴體內最終存活了758天。
心臟方面,原位移植(移除受體心臟)的最長存活時間為264天,異位心臟移植(不移除受體本身的心臟)的最長存活時間紀錄則達到了近1000天。
不過,無論是上述提到的5例活體異種器官移植手術中,還是人體到人體完成的移植器官,患者的術后生存率都還不盡如人意。
除去尚未披露治療結果的安徽醫科大學第一附屬醫院完成的異種肝移植手術,其余活體異種器官移植手術的患者最長存活時間僅為61天。USRDS 2021年度報告中闡述的同種移植手術數據顯示,公民逝世后器官捐獻/活體捐獻的腎移植后十年生存率為49.5%/65.5%,同樣存在極大的提升空間。
感染是腎移植術后早期死亡最常見的原因,與術后免疫抑制過度、營養不良及術后并發癥等有關。以免疫抑制過度為例,對于已經完成腎移植的患者,免疫抑制不足可能導致排斥反應,造成移植物結構損傷、移植物功能丟失、再移植困難;免疫抑制過度又會增加發生感染和腫瘤的風險。
此外,常用的免疫抑制劑(如環孢素、他克莫司、咪唑立賓等)治療效果穩定,但有不良反應多,治療方案局限等缺點。此外,生物免疫抑制劑價格昂貴,巨大的藥物治療費用也在一定程度上阻礙了手術患者的康復進展。
因此,長期、持續地關懷與照護對于此類患者非常重要,醫生需要對于患者的免疫狀態、移植器官狀態進行持續監測和調整,盡早發現問題并干預處理。另一方面,行業也需積極探索新型免疫抑制劑,在療效與衛生經濟學方面找到新的平衡點。
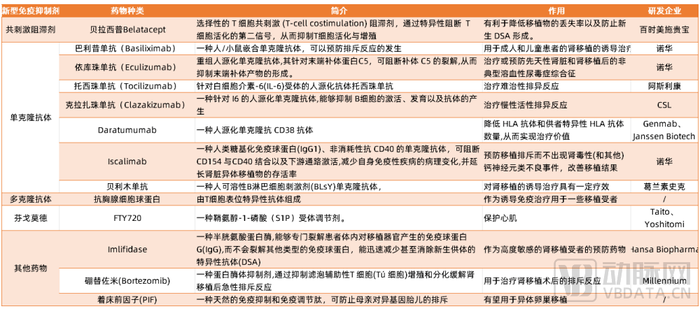
潛在的新型免疫抑制劑盤點
相較之下,異種移植排斥反應相關的基因約有30個,排斥反應更為復雜、更難克服,同時由于免疫抑制措施比同種移植更強,反過來對人體免疫系統的影響也更大,更容易導致固有免疫系統被破壞而發生感染,可能會引發嚴重并發癥。
在全球頭兩例異種器官移植案例中,Revivicor公司對供體豬實施了10項基因編輯操作,剔除了三個會引發人類快速抗體介導排斥反應的基因,還將六個與人類心臟免疫排斥相關的基因——CD46、CD55、血栓調節蛋白、內皮細胞蛋白C受體、CD47和血紅素加氧酶-1(HO-1)植入豬的基因組中,盡可能降低排斥反應的發生概率。
基因編輯大牛George Church創立的eGenesis為全球第三例活人異種移植手術培育了轉基因豬。這些豬經過了69項基因組編輯,敲除與豬細胞表面糖抗原合成相關的3個基因,轉入7個與排斥反應調節相關的人類基因,以便幫助豬細胞躲過人體免疫系統的盤查。同時,該公司還滅活了供體豬中的豬內源性逆轉錄病毒,以降低人類感染的風險。
但從結果來看,各個公司在基因編輯上的努力并未完全解決問題,異種移植排斥反應依然是阻礙異體器官移植的終極難關。
面對這一挑戰,新西蘭的NZeno,德國的Xtransplant,國內的中科奧格、蓋蘭德生物等初創企業也在積極入局,進行異種移植供體豬的培養,并已取得了非凡的成果。具體而言,他們以基因編輯技術構建低免疫原性供體豬,開發可供移植的豬紅細胞、皮膚、腎臟等組織器官治療技術,同時拓展基因編輯供體豬在生物材料再生醫學的應用,推動中國異體器官移植產業的發展。
寫在最后
作為醫學界的三大奇跡之一,器官移植最為完整地實現了人類生命高質量延續的夢想。只是,延續并非現代醫學的最終目的,數以萬計的研究者、醫生、患者參與其中,便是為了讓未來經歷移植的患者,實現真正意義上的重生。
實現這樣一個突破必然會經歷無數次的失敗,但每一次失敗均有其意義所在。正如全球首例豬心臟移植手術患者David Bennett的家人所說:
“我們對每一個創新時刻、每一個瘋狂的夢想、每一個不眠之夜心存感激,感謝所有為這項歷史性的手術付出努力的人,我們希望這個故事可以成為希望的開始,而不是結束。”
走在器官移植技術遷躍的邊緣,我們或許即將見證希望本身。


