文|動脈網
近年來,真實世界研究一再證明自己的價值。
無論是進行藥品、醫療器械上市后的相關評價,還是在特定條件下,作為藥品、醫療器械申報上市提供相關證據,真實世界研究吸引了大量頂級的科研團隊和開發企業。從過去幾年所取得的成績看,真實世界研究的應用優化了藥品、醫療器械的審批流程,也為大量臨床問題提供了解答。
那么,國內的真實世界研究應用,走到哪一步了?對于企業而言,布局真實世界研究是否就能穩賺不賠?我們試著討論這些問題。
真實世界研究形成閉環
單從概念看,真實世界研究是十分理想的試驗策略。避免了刻意的臨床試驗設計,可能提供比隨機對照試驗提供更客觀、豐富的數據,直接跟蹤患者治療情況,倫理層面也似乎更可行。但真實世界研究的應用探索真正熱起來,是在近幾年,尤其是當真實世界證據可用于產品注冊之后。
在國內,早期的的真實世界研究,主要被用來驗證與中醫藥相關的臨床問題。
據Pubscholar記載,在2010年,來自中國中醫科學院中醫臨床基礎醫學研究所的田峰和謝雁鳴兩位研究者,連發2篇文章,論述了真實世界研究在中藥上市后再評價中的價值。研究表明,在保證人民群眾用藥安全、有效的前提下,基于RWS的中藥上市后臨床再評價研究可能延長藥品的市場生命。
盡管只是純粹的理論研究,卻為國內真實世界研究奠定了邏輯基礎。隨后,關于燈盞細辛注射液、松齡血脈康膠囊、腹針、疏血通注射液等臨床上常見的中醫藥手段的真實世界研究陸續開展起來。
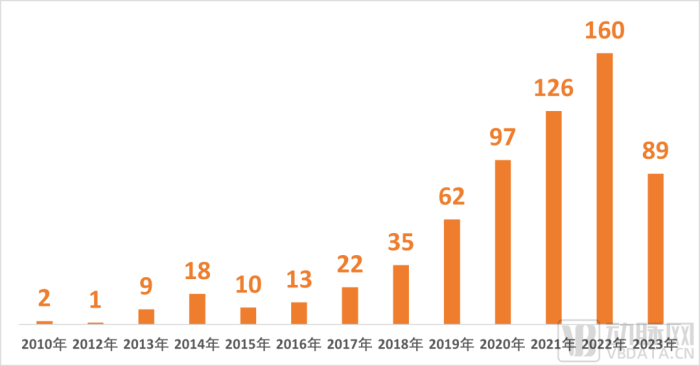
國內真實世界研究相關成果數量 數據來源:Pubscholar
在很長一段時間里,國內真實世界研究的熱度并不高。變化出現在2017年以后,越來越多創新的生物制劑,借助上市后的真實世界研究,來豐富臨床證據。根據Pubscholar數據,國內主流的高校和醫療機構,紛紛布局真實世界研究。
其中,中國中醫科學院中醫臨床基礎研究所的真實世界研究成果最豐富,達到11項。不過,純粹為上市后研究提供證據,真實世界研究對醫藥企業的吸引力有限,他們更加關注的,是產品注冊審批。

部分開展真實世界研究較多的高校 數據來源:Pubscholar
實際上,在國際上,利用真實世界研究來加速創新產品審批,已經有近半個世紀的歷史。
早在20世紀70年代,海外藥物監管部門就嘗試使用真實世界證據,來批準罕見疾病的新治療方案。2016年12月,美國食品藥品監督局FDA通過的《21世紀治愈法案》,真實世界研究走上了更大舞臺。在美國,真實世界證據,可以取代傳統臨床試驗,進行擴大適應證的批準。
此后,真實世界證據在全球藥品、醫療器械注冊申報中的應用生態越來越成熟。2017年8月開始的3年內,美國密集發布了大量真實世界證據的監管規則,包括《采用真實世界證據支持醫療器械的法規決策》、《臨床研究中使用電子健康檔案數據指南》、《真實世界證據方案框架》、《使用真實世界數據和真實世界證據向FDA遞交藥物和生物制品資料》等,來進一步完善與真實世界研究相關的監管規則體系。在這個過程中,歐盟藥品管理局、日本藥品和醫療器械管理局,也在多個層面體現對真實世界研究用于藥品研發和監管決策的關注和重視。
國內的真實世界研究審批創新藥和醫療器械實踐,始于海南樂城的醫療先行區試點。
2019年6月,國家藥監局與海南省政府聯合啟動海南臨床真實世界數據應用試點工作,嘗試將臨床真實世界數據用于醫療器械產品注冊。同年9月,國家四部委聯合發文支持博鰲樂城先行區發展,并明確提出“開展真實世界臨床數據應用研究”。隨后,將真實世界研究應用于藥品、醫療器械審批的相關規定體系,陸續建立起來。

國內部分真實世界研究相關政策 數據來源:動脈網根據公開信息整理
2019 年10 月,首批“真實世界研究”試點產品遴選啟動。但當時,國際藥械企業參與積極性并不高,最終只有3個產品入選,其中就包括艾爾建的青光眼引流管。入選后,艾爾建很快開始通過在樂城醫療先行區的臨床實踐,采集真實世界數據。據了解,艾爾建的青光眼引流管用于微創房水內引流術,當時已經在國外上市。
彼時,這款產品在國內還沒有同類產品。青光眼是世界排名第二的致盲性眼部疾病,被稱為“沉默的視力竊賊”,它所引發的視功能損傷,不可逆。艾爾建的青光眼引流管植入術步驟簡單,安全可控,無需破壞結膜及鞏膜組織,僅需透明角膜缺口即可輕松植入,有效避免了術中出血以及其他并發癥,顯著降低了手術風險。
2020年3月,艾爾建的青光眼引流管正式獲批在國內上市,成為國內首個使用境內真實世界數據獲批上市的醫療器械。而這距離對應的真實世界研究啟動,還不到5個月。此前,在傳統申報方式之下,擬進口產品需要經過嚴格的臨床試驗,往往至少耗時3至5年。
艾爾建青光眼引流管上市的2個月后,樂城醫療先行區的第二批“真實世界研究”試點產品申報啟動。青光眼引流快的急速獲批,瞬間點燃了國際藥械巨頭的熱情,共有47個進口醫療器械品種申報進入第二批試點。
2022年6月,歐康維視生物開發的治療慢性非感染性葡萄膜炎產品OT-401(氟輕松玻璃體植入劑),在國內獲批上市,成為國內藥品注冊史上第一個完全基于真實世界研究數據申報和獲批上市的新藥。2018年10月,OT-401獲批在美國上市,用于治療累及眼后段的慢性非感染性葡萄膜炎,是FDA在當時唯一批準的、可釋放氟輕松長達36個月的用于治療慢性非感染性葡萄膜炎的新藥。
在國內,葡萄膜炎是第二大致盲性眼病,原有的解決方案難以幫助患者長時間穩定葡萄膜炎炎癥,避免反復發作引發眼內組織損傷,用藥依從性較差。歐康維視生物從OT-401的原研藥廠EyePoint Pharmaceuticals手中,取得了這款產品在大中華地區的獨家開發和商業化權利。OT-401通過真實世界研究快速上市,無疑填補了國內慢性非感染性葡萄膜炎治療領域的空白。
至此,真實世界證據在國內藥品、醫療器械的注冊審批、上市后評價等場景,都有了應用,閉環的生態正在形成。
巨頭的搶跑
根據剛剛結束的第二屆博鰲國際藥械真實世界研究大會數據,過去 3 年間,在樂城醫療先行區的真實世界數據應用試點中,累計有13個試點品種獲批上市,試點范圍覆蓋腫瘤、免疫、眼科等多個領域。2023年4月開始,樂城醫療先行區地醫療器械真實世界研究進入常態化,更多創新醫療器械品種申請納入真研前置溝通渠道。

國內部分基于真實世界研究獲批的產品 數據來源:動脈網根據公開信息整理
值得注意的是,真實世界研究已經成為跨國醫藥巨頭進入國內市場的重要方式,除了已經基于真實世界證據,將創新的全球產品送到國內的醫院中的艾爾建、強生、波士頓科學、諾華制藥等企業外,輝瑞、默沙東、賽默飛等跨國醫藥企業也紛紛布局真實世界研究。
采用真實世界研究的路徑,跨國企業往往能在藥械上市后3年左右,讓新產品進入國內市場,這對于斥重金做研發的跨國醫藥企業而言,至關重要。比如,艾爾建的青光眼引流管從美國上市到中國上市,間隔不到4年,強生的白力士、波士頓科學的蒸汽治療設備,則間隔不到3年,諾華制藥的英克司蘭鈉注射液,兩地上市間隔時間更是縮短到2年以內。
更重要的是,搶跑進入國內市場的創新藥械,由于填補了臨床空白,市場滲透的速度通常相當快。比如,心血管領域的國際首個小干擾核酸藥物英克司蘭鈉注射液,2021年7月在樂城實現全國首例應用,僅一年多時間累計使用7000余例次。而2022年3月正式獲批上市得波士頓科學的試點品種熱蒸汽治療設備和一次性使用前列腺熱蒸汽治療器械,已經在全國100余家醫療機構使用,累計治療約1000名前列腺增生患者。
2023年8月,諾華制藥的新型降膽固醇藥物英克司蘭鈉注射液獲國家藥監局批準上市,這是樂城醫療先行區的臨床真實世界數據應用試點中,獲批上市的第4個藥品。
英克司蘭鈉注射液主要用于成人原發性高膽固醇血癥(雜合子型家族性和非家族性)或混合型血脂異常患者的治療等。2021年8月,該產品進入博鰲樂城臨床真實世界數據應用試點。從提交注冊申請到獲批上市,僅歷時9個多月,極大縮短了該產品進入中國市場的時間。
2023年以來,更多的跨國醫藥企業搶灘真實世界研究。他們一方面以樂城先行區為據點,拓展真實世界研究的業務邊界,另一方面則加強與國內醫療機構的真實世界研究合作。
2023年5月,賽諾菲與海南樂城真實世界研究院簽訂戰略合作協議,雙方將通過開展創新產品先行先試、真實世界研究、舉辦學術交流等,推動創新產品落地。此外,在第六屆進博會上,輝瑞中國也海南樂城真實世界研究院、暨南大學粵港澳大灣區藥品醫療器械真實世界研究院、華潤廣東醫藥有限公司簽訂戰略合作協議,方將共同促進海外及香港上市的創新藥物在海南博鰲樂城先行區、大灣區開展真實世界研究,推動創新藥物審評加速。羅氏診斷中國、羅氏制藥中國則攜手上海交通大學醫學院附屬瑞金醫院,共同發布淋巴瘤診療方案,協力推進 DLBCL 治療的多中心臨床的大型真實世界研究。
相比之下,默沙東的布局則更深。11月6日,默沙東(海南)創新醫療有限公司在進博會上揭牌,成為首個進入海南省的跨國醫藥企業子公司。而在此之前,默沙東就一直在樂城醫療先行區從事真實世界研究。2020年7,默沙東中國與樂城管理局簽署備忘錄,雙方在樂城先行開展真實世界研究等方面加深合作達成共識。2023年3,默沙東成為海南樂城真實世界研究院理事成員單位,積極共建海南樂城真實世界研究院,推動真實世界研究科創孵化工作。
Biotech彎道超車?
動脈網注意到,除了跨國醫藥企業外,國內的Biotech也從真實世界研究中獲益。
2021年3月,基石藥業開發的普拉替尼膠囊,基于真實世界研究證據,在國內獲批上市,用于既往接受過含鉑化療的轉染重排(RET)基因融合陽性的局部晚期或轉移性非小細胞肺癌(NSCLC)成人患者。這是國內獲批的首個RET抑制劑,也是基石藥業在IPO兩年后。迎來的首個商業化產品。從基石藥業最新的財報看,搶跑上市的普拉替尼膠囊,成為這家未盈利Biotech的主要收入來源。
普拉替尼上時候的第一個完整年度,根據基石藥業2022年年報,共實現收入4.81億元,較上年幾乎翻倍,普拉替尼作為三款商業化的產品之一,功不可沒。而根據基石藥業2023年半年報,2023年前6個月,共實現收入2.615億元,相比2022年同期,增長53%。
同樣通過真實世界研究上市的OT-401,也成為未盈利的歐康維視生物的主要收入來源。根據歐康維視生物 2022 年財報,在OT-401 上市當年,公司總收入從 5614.6 萬元增長至 1.58億元,增幅近3倍。歐康維視生物還表示,OT-401有望為 2023 年的銷售業績帶來有力支撐。
不過,醫藥企業想要通過真實世界研究,推動產品快速上市,門檻并不低。從已經獲批上市的13款產品來看,技術領先、臨床急需,是基本要求。而在具體的審批實踐中,對于可以參與真實世界研究,并基于真實世界證據申報產品注冊,門檻并不低。
具體而言,一方面,基于真實世界證據申報注冊的產品,通常具備了相當充足的海外臨床研究數據,而真實世界數據僅用作輔助證據。比如,在樂城醫療先行區開展真實世界研究前,歐康維視生物的OT-401在境外已經完成的三期臨床試驗數據,普拉替尼申請上市提交的主要數據也來自海外,樂城醫療先行區的真實世界數據則為普拉替尼在中國晚期非小細胞肺癌人群中的療效評價和安全性評估提供了輔助。
另一方面,現階段,對于大多數藥物、醫療器械和疾病而言,真實世界研究的試驗設計還沒有標準化的方案,這就需要真實世界研究的開辦者具有豐富的臨床實驗和數據分析經驗,否則將很難成功,畢竟利用真實世界數據向國家藥監局申請上市的前提,是數據要達到主要終點指標,體現出統計學的差異。
動脈網查詢公開信息發現,歐康維視生物提交給國家藥監局的 OT-40申報資料,是真實世界數據研究中的28例受試者數據,而基石藥業授權引進的普拉替尼也使用了樂城9例受試者的真實世界數據申報上市。此前有媒體分析,真實世界研究的方案設計,既要考慮產品本身的臨床價值,也要考慮涉及的國內人群特點,難度非常大。
不可否認,將真實世界研究作為創新醫藥產品上市申報的輔助工具,減輕了藥企和醫療器械企業的研發壓力,也拉進了患者與最先進療法之間的距離。但醫療畢竟是非常嚴肅的工作,真實世界數據如果要發揮更重要的價值,無疑還需要更嚴厲的監管,和更充足的臨床證據。


